
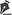
Original Article - Year 2013 - Volume 28 -
Retalho toracodorsal desepitelizado: um novo conceito para a reconstrução autóloga da mama
Deepithelialized thoracodorsal flap: a new concept for autologous breast reconstruction
RESUMO
INTRODUÇÃO: A associação de retalho muscular toracodorsal com uma extensão fasciocutânea resulta em um amplo retalho, que permite recobrir o defeito cutâneo residual da mastectomia. O objetivo deste estudo é compartilhar 11 anos de experiência com um novo conceito em reconstrução autóloga da mama, utilizando um retalho cutâneo toracodorsal desepitelizado pediculado com músculo grande dorsal como vetor.
MÉTODO: Foi realizado um estudo retrospectivo com 247 pacientes operadas de 1999 a 2009. Os parâmetros de interesse incluíram idade, índice de massa corporal, história de tabagismo, radioterapia e quimioterapia, tamanho da mama, dimensões do retalho, tempo cirúrgico, expansão do tecido mamário e índice de complicações. O desenho do retalho toracodorsal em formato de elipse se estende da região da linha dorsal média até a linha inframamária média, com largura máxima na linha axilar média. A extensão fasciocutânea desepitelizada é colocada dissecada juntamente com o músculo grande dorsal como seu veículo e pedículo responsável pelo suprimento sanguíneo, que são levados em monobloco até a área de pele da nova neomama previamente dissecada. O formato e a projeção da mama são restaurados gradualmente como uma expansão de tecido.
RESULTADOS: Reconstruções imediata e tardia da mama foram realizadas em 14,5% e 85,5% das pacientes, respectivamente. A reconstrução bilateral da mama foi realizada em 8,9% das pacientes. Nenhuma das pacientes submetidas a radioterapia mamária (76,7%) recebeu implantes para reconstrução. O tempo cirúrgico médio foi de 2 horas e 20 minutos. A expansão da pele mamária não irradiada foi realizada em um período de 3 meses, enquanto a expansão da pele irradiada levou um período médio de 5 meses após a reconstrução tardia. A taxa de complicações foi de 11,3%. Não houve perda total do retalho. A taxa de seroma foi de 7% após a remoção dos drenos. O tempo de hospitalização médio foi de 3 dias. Foi realizado remodelamento da mama contralateral em 92% dos casos e enxerto de gordura em 14% das pacientes. Em um período médio de acompanhamento de 4 anos, a taxa de satisfação das pacientes foi elevada.
CONCLUSÕES: O retalho toracodorsal é uma opção cirúrgica segura e confiável para a reconstrução autóloga da mama. As principais vantagens são a obtenção de grandes volumes de mama contornando o uso de material protético, evitando-se a aparência de retalho na mama reconstruída, obtendo-se expansão tecidual e, ao mesmo tempo, garantindo morbidade aceitável no sítio doador.
Palavras-chave: Mama/cirurgia. Mamoplastia/métodos. Retalhos cirúrgicos.
ABSTRACT
BACKGROUND: The association the thoracodorsal muscular flap with a thoracic fascio-cutaneous extension results in a large flap, that allowed to cover the mastectomy residual skin defect. The purpose of this study is to share 11 year experience with a new concept in autologous breast reconstruction using a deepithelialized thoracodorsal skin flap pedicle with the latissimus dorsi muscle as vector.
METHODS: A retrospective study of 247 operated patients from 1999 to 2009 was performed. Parameters of interest included age, body mass index, smoking, radiation and chemotherapy histories, breast size, flap dimensions, operative time, breast tissue expansion and complication rates. The thoracodorsal flap design under an ellipse shape extends from near the mid dorsal line extended up to the mid-infra-mammary line with maximal width at the mid axillary line. The deepithelialized fascio-cutaneous extension is lumped together with the latissimus dorsi as its vehicle and blood supply pedicle, together are brought to the neo-mammary previous dissected skin area. Gradual as a tissue expansion the breast shape and projection are restored.
RESULTS: Immediate and delayed breast reconstructions were done in 14.5% and 85.5%, respectively. Bilateral breast reconstruction was done in 9% of the patients. Implants were not used for reconstruction purposes in any of the 77% of the patients received breast radiotherapy. The average operative time was 2 hours and 20 minutes. Expansion of non irradiated breast skin occurred over a three months period, whereas that of irradiated skin took an average of five months following delayed reconstruction. The complication rate was 11.4%. No total flap loss was reported. The seroma rate was 7% after the drains had been removed. The mean hospital stay was 3 days. Contra lateral breast remodeling was performed in 92% of the cases and fat grafting in 14% of the cases. With an average follow-up of 4 years, patient satisfaction was rated high by the patients.
CONCLUSIONS: The thoracodorsal flap is a safe and reliable surgical option for autologous breast reconstruction. Its main advantages achieving large breast volumes circumventing the use of prosthetic material, avoiding the patch look on the reconstructive breast, achieving tissue expansion, while insuring acceptable donor site morbidity.
Keywords: Breast/surgery. Mammaplasty/methods. Surgical flaps.
Após a primeira descrição do retalho do músculo grande dorsal por Tansini, em 1896, seu uso oscilou e teve seu entusiasmo renovado na década de 1970, após melhor compreensão dos retalhos cutaneomusculares1,2. O músculo grande dorsal continuou sendo a principal fonte de retalho na cirurgia de reconstrução mamária até a introdução do retalho transverso do músculo reto abdominal (TRAM), em 1982, acompanhado de maior exploração de retalhos livres e perfurantes3-6. O retalho do grande dorsal tornou-se uma segunda opção para a reconstrução mamária, e modificações do retalho ressurgiram nas últimas 3 décadas, com o objetivo de reavivar seu uso5-17. Apesar das diferentes modificações incorporadas ao retalho do músculo grande dorsal, ainda havia grandes limitações, incluindo persistência da aparência de retalho em reconstruções tardias, em decorrência da quantidade limitada e da flexibilidade da pele disponível sobre a mama tratada. Além disso, o volume limitado proporcionado pelo retalho dissecado determinava a necessidade de implantes aloplásicos, para obtenção dos volumes desejados. Com base nesse contexto, a combinação de retalho muscular toracodorsal com uma extensão fasciocutânea resulta em amplo retalho, que permite recobrir o defeito cutâneo residual da mastectomia. O ponto-chave é evitar o uso de implante adicional.
O objetivo deste estudo é compartilhar 11 anos de experiência com um novo conceito em reconstrução autóloga da mama, utilizando um retalho cutâneo toracodorsal desepitelizado pediculado com músculo grande dorsal como vetor.
MÉTODO
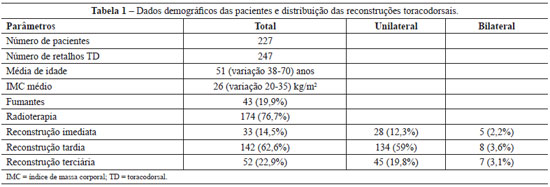
Foi realizado um estudo retrospectivo dos bancos de dados para identificar as pacientes submetidas a reconstrução com retalho toracodorsal após mastectomia entre 1999 e 2009. Todas as pacientes foram operadas pelo mesmo cirurgião sênior. Os parâmetros de interesse incluíram idade, índice de massa corporal (IMC), história de tabagismo, radioterapia e quimioterapia, tamanho da mama, dimensões do retalho, tempo cirúrgico, expansão do tecido mamário e índice de complicações.
A idade das pacientes variou de 38 anos a 70 anos, com média de 51 anos, e o IMC variou entre 20 kg/m2 e 34 kg/m2, com média de 26 kg/m2. Quarenta e três (19%) pacientes eram fumantes ativas.
As principais indicações para o retalho toracodorsal incluíram a preferência das pacientes pela reconstrução autóloga com contraindicações para retalho abdominal, rejeição das pacientes à aparência de retalho da mama reconstruída, falha de modalidades anteriores de tratamento, incluindo outros tipos de reconstrução autóloga, além do implante de próteses.
Foram incluídas pacientes submetidas a reconstrução imediata ou tardia, unilateral ou bilateral, além de implantes de próteses, com ou sem radioterapia e/ou implantes mamários.
Os critérios de exclusão compreenderam lesão cutânea grave secundária a radioterapia mamária, com necessidade de excisão da pele lesionada e perda de acompanhamento um ano após a cirurgia. Os dados foram integrados e analisados em um banco de dados computadorizado (Tabela 1).
Demarcação do Retalho Cutâneo
O retalho é desenhado em formato elíptico transversal, com a paciente em posição ereta. A elipse se estende 2 cm a 3 cm em posição lateral da linha média das costas até a dobra inframamária média. A metade superior do segmento das demarcações cutâneas permanece na projeção do músculo grande dorsal e a metade inferior, nas projeções dos músculos serrátil e oblíquo. A maior dimensão do retalho localiza-se na linha axilar média (Figura 1). O pinçamento manual (pinch test) é utilizado para estimar a largura do retalho.
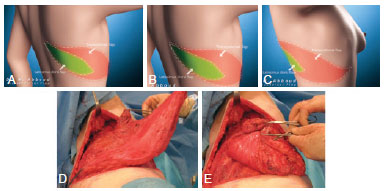
Figura 1 - Em A, B e C, aspectos esquemáticos da demarcação do músculo grande dorsal e o retalho grande dorsal integrados em monobloco. O retalho cutâneo é desepitelizado em toda sua extensão, com cerca de 35 cm de comprimento, e o pinch test no sentido transversal varia entre 12 cm e 15 cm. Em D e E, ressecção da extensão do músculo grande dorsal junto ao colo do úmero para sua mobilização.
O suprimento neurovascular para os retalhos cutâneo e do grande dorsal é feito pelo ramo terminal da artéria subescapular, que é um ramo do terço médio da artéria subescapular. Essa artéria subescapular também se divide em artéria circunflexa escapular e artéria toracodorsal. Uma vez que penetra o músculo e corre paralela às fibras musculares e seus vasos perfurantes, a artéria toracodorsal vasculariza toda a pele que está acima. A inserção do tendão do músculo grande dorsal pode ser seccionada na inserção do úmero sem causar danos ao feixe.
Técnica Cirúrgica
As pacientes são operadas na posição lateral, com o braço colocado em abdução de 90 graus, sob anestesia geral e intubação traqueal. A incisão da pele é realizada ao longo das marcações prévias e a desepitelização, em toda a extensão do retalho, exceto nos casos de reconstrução mamária imediata, para preservar um pequeno segmento de pele para a reconstrução do complexo aréolo-mamilar no mesmo estágio.
A dissecção cutânea expõe o músculo grande dorsal, que é dissecado em toda sua extensão, seccionando o tendão em todos os casos. O músculo grande dorsal e o retalho cutâneo desepitelizado continuam conectados à estrutura vascular preservada e ao nervo, também intacto. As duas extremidades de retalho cutâneo e os segmentos do músculo grande dorsal, incluindo seu tendão, são suturados unidos por 2 a 3 pontos não-absorvíveis isolados, formando um monobloco e rodados a 180 graus. A dissecção do acesso à mama é realizada a partir da mesma incisão do sítio doador, criando-se uma bolsa para inserção do retalho. É feita uma avaliação do tecido cicatricial ou capsulectomia sempre que necessário nesse estágio. O retalho é então inserido na bolsa e fixado à dobra inframamária utilizando uma sutura simples. O ápice do retalho, contendo o tendão muscular, também é levado em direção à extremidade da mama e fixado ali para evitar possível tensão. São posicionados 3 drenos de sucção nas regiões torácica e axilar. As bordas da ferida do sítio doador são suturadas por pontos isolados em planos multicamadas. As pacientes são posicionadas em posição supina e a camada de pele do retalho é exteriorizada para reconstruir o complexo aréolo-papilar. A sutura cutânea final é realizada na face lateral da mama e recoberta por uma bandagem esterilizada. As pacientes são orientadas a utilizar sutiã compressivo 48 horas após a cirurgia e sutiã convencional por 1 a 3 meses.
As Figuras 2 a 7 ilustram a técnica descrita neste trabalho.
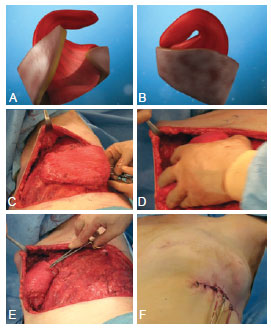
Figura 2 - Em A e B, aspecto esquemático e anatômico do retalho dermomuscular e do segmento livre do músculo dorsal em monobloco, suturados pelas extremidades. Em C, aspecto do retalho girado 180 graus, seguido de sua inclusão na bolsa cutânea da região da neomama previamente dissecada em toda sua área. Em D, introdução do retalho mobilizado no leito receptor. Em E, pontos isolados com fio não-absorvível fixam a face dérmica do retalho ao músculo serrátil. Em F, aspecto da sutura cutânea e posicionamento de 3 drenos de sucção, um na axila e os outros dois na região dissecada no tórax.
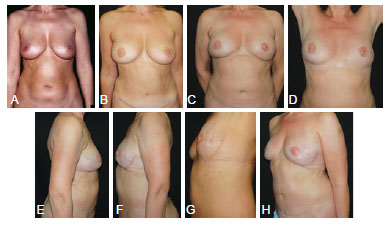
Figura 3 - Caso de câncer de mama esquerda, 4 anos após reconstrução com retalho TRAMpara tratamento de câncer de mama direita. Em A, aspecto pré-operatório de paciente submetida a reconstrução com retalho TRAM em mama direita, em vista frontal. Em B,aspecto pós-operatório um ano depois do procedimento, em vista frontal. Em C a H, aspecto pós-operatório de paciente submetida a reconstrução com retalho toracodorsal em mama esquerda, no acompanhamento de 5 anos, em vista frontal (C), com os braços levantados (D), em perfil direito (E), em perfil esquerdo (F e G), e em oblíqua esquerda (H).
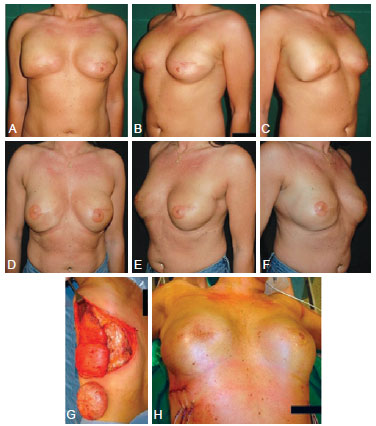
Figura 4 - Em A a C, aspecto pré-operatório de paciente submetida a reconstrução mamária tardia bilateral utilizando implantes, com história de radioterapia nas duas mamas. Em D a F, aspecto 3 anos após remoção dos 2 implantes e reconstrução mamária com retalhos toracodorsais bilaterais, sem emprego de implantes. Em G e H, aspecto intraoperatório demonstrando o volume proporcionado pelo retalho, duplicando o tamanho do implante.
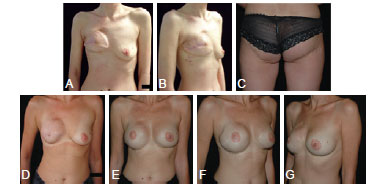
Figura 5 - Em A e B, aspecto pré-operatório de paciente que apresentou falha da reconstrução da mama direita com retalhos glúteos bilaterais livres, reconstrução protética com contratura capsular secundária. A paciente foi submetida a radioterapia na mama direita. Em C, aspecto do sítio doador da primeira reconstrução. Em D a G, aspecto 4 anos após remoção do implante e reconstrução da mama direita com retalho toracodorsal, seguida por aumento bilateral com prótese, realizado posteriormente.
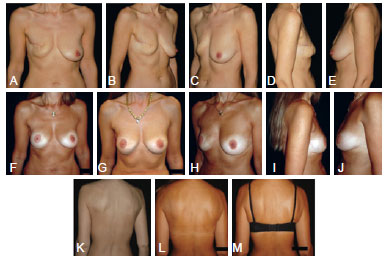
Figura 6 - Em A a E, aspecto pré-operatório de paciente submetida a reconstrução tardia da mama direita com retalho toracodorsal em mama tratada previamente com radioterapia. Em F a J, aspecto pós-operatório de 5 anos. Em K a M, a comparação dos aspectos pré-operatório (K) e pós-operatório (L e M), demonstrando que a cicatriz do sítio doador fica escondida na linha do sutiã.
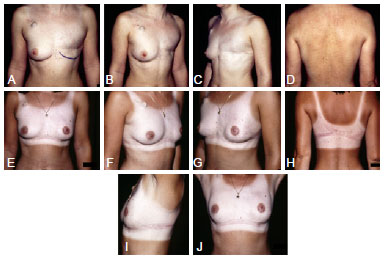
Figura 7 - Em A a D, aspecto pré-operatório de paciente submetida a reconstrução tardia da mama esquerda com retalho toracodorsal. A paciente havia realizado radioterapia na mama esquerda. Em D a I, aspecto pós-operatório de 2 anos.
RESULTADOS
O número total de retalhos toracodorsais foi de 247 em 227 pacientes, após exclusão de 9 pacientes que não completaram o acompanhamento pós-operatório mínimo de 1 ano. Foram excluídas, também, 7 (3,1%) pacientes que apresentavam problemas cutâneos graves secundários à radioterapia mamária, exigindo excisão da pele lesionada.
A população estudada foi uma combinação das pacientes submetidas a reconstrução imediata (14,5%), reconstrução tardia (85,5%), unilateral (91,1%) ou bilateral (8,9%). Cinquenta e dois pacientes haviam sido submetidas a reconstrução mamária prévia com implantes, que foram removidos em todos os casos e substituídos por retalhos toracodorsais. Um total de 174 (76,7%) pacientes recebeu radioterapia mamária.
As dimensões do retalho variaram de 11 cm a 16 cm de largura e de 32 cm a 43 cm de comprimento, com média de 13 cm e 18 cm, respectivamente. A maioria das mamas obtidas era de taça C, variando de B a D. O tempo cirúrgico médio foi 140 minutos, variando entre 120 e 180 minutos (Tabela 2).
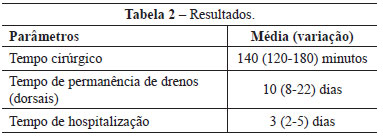
A taxa de complicação global foi de 11,3% nesta série. Não foram registradas perdas de retalho. As complicações incluíram 16 (7%) casos de seroma, 6 (2,6%) infecções da ferida cirúrgica, 3 (1,3%) hematomas e 1 (0,4%) deiscência da ferida no sítio doador (Tabela 3). Todas as complicações foram tratadas de forma conservadora. A duração da hospitalização variou entre 2 dias e 5 dias, com média de 3 dias. Os drenos torácicos e axilares foram removidos entre 3 dias e 7 dias de pós-operatório (média de 4 dias). O dreno dorsal foi mantido por 8 dias a 22 dias de pós-operatório (média de 10 dias). O período de acompanhamento médio foi de 4 anos, variando de 1 ano a 10 anos. O remodelamento da mama contralateral na forma de mastopexia, redução ou lipoaspiração mamária simples foi realizado em 92% dos casos, sendo o lipopreenchimento da mama reconstruída realizado em 14% dos casos.

Não foi utilizada prótese para reconstrução. Entretanto, implantes mamários bilaterais foram colocados em 41 (18,1%) casos por solicitação das pacientes, apenas para aumentar o volume das mamas como um procedimento estético secundário após reconstrução autóloga.
DISCUSSÃO
O retalho do músculo grande dorsal continua sendo uma ferramenta versátil na cirurgia de reconstrução mamária; contudo, o volume limitado e a persistência do efeito de retalho na mama reconstruída constituem seus principais pontos fracos. Muitos autores tentaram solucionar esses inconvenientes com a proposição de modificações do retalho do músculo grande dorsal6-18. Em 1987, foi descrito um procedimento com retalho total do músculo grande dorsal obtido ressecado com grande camada de pele8. A liberação completa ou parcial do tendão do retalho grande dorsal de sua inserção umeral facilita a rotação e o posicionamento do retalho com menos volume na axila9,13,19,20. Ao trazer o músculo junto com o retalho no intraoperatório, utilizando pontos simples, garantimos uma mama mais volumosa e também reduzimos a força das contrações musculares. Concordamos com outros autores que defendem a fixação do retalho à parede torácica para reduzir a tensão no pedículo13,20. Na verdade, não observamos sequelas como torção ou tensão excessiva que pudessem afetar a viabilidade do retalho. Certamente existem armadilhas nessa manobra, incluindo-se a contração muscular incômoda, a qual é reduzida com o passar do tempo13,19,21.
A incidência de seroma foi baixo em comparação à literatura, o que pode ser explicado pelo fato de essa complicação ser registrada somente após a remoção dos drenos9,10,11,13. Apesar do uso de várias manobras conhecidas para reduzir a incidência de seroma, incluindo-se pontos de adesão e fechamento sem tensão em múltiplas camadas do sítio doador, os drenos foram mantidos, em média, por 10 dias, e ainda assim houve seroma.
Semelhante a outras técnicas cirúrgicas, o retalho do músculo grande dorsal tem suas desvantagens. A cicatriz longa do sítio doador e a discreta deformidade no contorno das costas são as principais limitações dessa modalidade cirúrgica. Além disso, o aprofundamento da totalidade do retalho na reconstrução tardia prejudica o monitoramento de parâmetros como congestão venosa, entre outras complicações de curto prazo. Esse não foi um grande obstáculo, já que não houve perdas totais do retalho na população deste estudo. As contraindicações para emprego dessa técnica incluem toracotomia prévia no lado da reconstrução, assim como lesão cutânea grave secundária a doses de radiação consideráveis, impedindo expansão adequada do tecido.
CONCLUSÕES
O retalho toracodorsal é uma técnica cirúrgica segura e confiável com uma ampla variedade de aplicações na reconstrução mamária após mastectomia com ou sem radiação. Além de servir como retalho de resgate quando outras modalidades de tratamento falham, suas principais vantagens incluem obtenção de adequados volumes mamários, evitando o uso de material protético, melhora da qualidade da pele, principalmente após radiação, e expansão tecidual considerável sem necessidade de expansores, além de garantir morbidade mínima ao sítio doador. O retalho toracodorsal é uma boa opção cirúrgica para a reconstrução mamária após mastectomia, principalmente na mama irradiada.
REFERÊNCIAS
1. Mathes SJ, Nahai F. Clinical atlas of muscle and musculocutaneous flaps. St Louis: Mosby; 1980.
2. Schneider WJ, Hill HL Jr., Brown RG. Latissimus dorsi myocutaneous flap for breast reconstruction. Br J Plast Surg. 1977;30(4):277-81.
3. Fujino T, Harashina T, Enomoto K. Primary breast reconstruction after a standard radical mastectomy by a free flap transfer. Case report. Plast Reconstr Surg. 1976;58(3):371-4.
4. Koshima I, Soeda S. Inferior epigastric artery skin flaps without rectus abdominis muscle. Br J Plast Surg. 1989;42(6):645-8.
5. Marshall DR, Anstee EJ, Stapleton MJ. Soft tissue reconstruction of the breast using an extended composite latissimus dorsi myocutaneous flap. Br J Plast Surg. 1984;37(3):361-8.
6. Barnett GR, Gianoutsos MP. The latissimus dorsi added fat flap for natural tissue breast reconstruction: report of 15 cases. Plast Reconstr Surg. 1996;97(1):63-70.
7. Hokin JA. Mastectomy reconstruction without a prosthetic implant. Plast Reconstr Surg. 1983;72(6):810-8.
8. Hokin JA, Silfverskiold KL. Breast reconstruction without an implant: results and complications using an extended latissimus dorsi flap. Plast Reconstr Surg. 1987;79(1):58-66.
9. Papp C, Zanon E, McCraw J. Breast volume replacement using the de-epithialized latissimus dorsi myocutaneous flap. Eur J Plast Surg. 1988;11(3):120-5.
10. McCraw JB, Papp CT. Latissimus dorsi myocutaneous flap: "fleur-de-lis" reconstruction. In: Hartrampf CR, ed. Breast reconstruction with living tissue. Norfolk: Hampton Press; 1991. p.221.
11. Aitken ME, Mustoe TA. Why change a good thing? Revisiting the fleur-de-lis reconstruction of the breast. Plast Reconstr Surg. 2002;109(2):525-38.
12. Germann G, Steinau HU. Breast reconstruction with the extended latissimus dorsi flap. Plast Reconstr Surg. 1996;97(3):519-26.
13. Chang DW, Youssef A, Cha S, Reece OR Autologous breast reconstruction with the extended latissimus dorsi flap. Plast Reconstr Surg. 2002;110(3):751-61.
14. Rifaat MA, Amin AA, Bassiouny M, Nabawi A, Monib S. The extended latissimus dorsi flap option in autologous breast reconstruction: a report of 14 cases and review of the literature. Indian J Plast Surg. 2008;41(1):24-33.
15. Heitmann C, Relzer M, Kuentscher M, Menke H, Oermann O. The extended latissimus dorsi flap revisited. Plast Reconstr Surg. 2003;111(5):1697-701.
16. Hudson DA, Ndobe E. Using two flaps to achieve aesthetic autologous breast mound reconstruction. Ann Rlast Surg. 2002;49(2):189-92.
17. Delay E, Jorquera F, Pasi P, Gratadour AC. Autologous latissimus breast reconstruction in association with the abdominal advancement flap: a new refinement in breast reconstruction. Ann Plast Surg. 1999;42(1):67-75.
18. Menke H, Erkens M, Olbrisch RR. Evolving concepts in breast reconstruction with latissimus dorsi flaps: results and follow-up of 121 consecutive patients. Ann Rlast Surg. 2001;47(2):107-14.
19. Delay E, Gounot N, Bouillot A, Zlatoff P, Rivoire M. Autologous latissimus breast reconstruction: a 3-year clinical experience with 100 patients. Rlast Reconstr Surg. 1998;102(5):1461-78.
20. McCraw JB, Papp C, Edwards A, McMellin A. The autogenous latissimus breast reconstruction. Clin Rlast Surg. 1994;21(2):279-88.
21. Slavin SA. Improving the latissimus dorsi myocutaneous flap with tissue expansion. Rlast Reconstr Surg. 1994;93(4):811-24.
1. Cirurgião plástico, chefe da Divisão de Cirurgia Plástica do Centro Hospitalar Universitário de Tivoli, La Louvière, Bélgica
2. Cirurgião plástico do Centro Médico da Universidade Americana de Beirute, Departamento de Cirurgia, Divisão de Cirurgia Plástica Reparadora e Estética, Beirute, Líbano
3. Cirurgião plástico, membro titular da Sociedade Brasileira de Cirurgia Plástica, editor-chefe da Revista Brasileira de Cirurgia Plástica, Campinas, SP, Brasil
Correspondência para:
Marwan Abboud
Rue du Magistrat, 7
Bruxelles, Belgique - 1000
E-mail: info@maclinic.eu
Artigo submetido pelo SGP (Sistema de Gestão de Publicações) da RBCP.
Artigo recebido: 8/1/2013
Artigo aceito: 22/3/2013
Trabalho realizado na clínica privada do autor principal, Bruxelas, Bélgica.


 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter