
Original Article - Year 2016 - Volume 31 -
Lipoenxertia subcicatricial associada à rigottomy: uma análise clínica e microestrutural
Subcicatricial fat grafting associated with rigotomy: a clinical and microstructural analysis
RESUMO
INTRODUÇÃO: O aumento da sobrevida na fase aguda do paciente grande queimado faz também aumentar a prevalência das sequelas cicatriciais estético-funcionais. Ao pensarmos na relevância clínica da lipoenxertia subcicatricial, necessita-se da compreensão e avaliação microscópica das reais alterações após o procedimento.
MÉTODOS: Foram selecionados oito pacientes, vítimas de queimadura por álcool, com tempo médio após queimadura de 12 meses (10-14 meses), sendo submetidos à lipoenxertia subcicatricial associada à Rigottomy. Foram realizadas biópsias cutâneas no pré e pós-operatório tardio com 14 semanas. Avaliados os quesitos: 1 - Melhora estético funcional da cicatriz pela escala de Vancouver; 2 - Análise quantitativa e qualitativa do colágeno cicatricial; 3 -Análise imunohistoquímica da vascularização cicatricial com anti-fator de crescimento derivado do endotélio vascular (antiVEGE).
RESULTADOS: Ao compararmos o período pré e pós-lipoenxertia, pôde-se avaliar que houve melhora estético-funcional significativa e, microscopicamente, redefinição entre os limites da derme papilar e reticular; redução quantitativa e reorganização do colágeno, além do decréscimo da vascularização tecidual pela análise imunohistoquímica.
CONCLUSÃO: O princípio básico de todo processo cicatricial fisiológico é reestabelecer a homeostasia local, ou seja, as etapas exageradamente intensificadas levam a alterações clínicas catastróficas. Ao realizar a lipoenxertia subcicatricial associada à Rigotomia, foi verificada, neste estudo, a melhora qualitativa e quantitativa do tecido. Sendo assim, torna-se evidente o futuro promissor deste procedimento para a complementação terapêutica das patologias cicatriciais.
Palavras-chave: Enxerto de pele; Cicatriz; Queimaduras; Cicatrização; Procedimentos cirúrgicos reconstrutivos.
ABSTRACT
INTRODUCTION: The increase in survival of large burn patients during the acute phase has also increased the prevalence of esthetic-functional scarring sequelae. With regard to the clinical relevance of subcicatricial fat grafting, the actual changes after the procedure need to be understood and microscopically evaluated.
METHODS: Eight patients with alcohol burns, with an average time after burn of 12 months (10-14 months), who underwent subcicatricial fat grafting associated with rigotomy were selected. Skin biopsies were performed in before and 14 weeks after operation. The following issues were assessed: 1) esthetic-functional improvement of the scar, by using the Vancouver scar scale; 2) quantitative and qualitative analyses of cicatricial collagen; 3) immunohistochemical analysis of scar vascularization with anti-vascular endothelial growth factor (anti-VEGF) antibody.
RESULTS: When comparing the pre- and post-fat grafting period, a significant esthetic-functional improvement and, microscopically, a redefinition of the boundaries of the papillary and reticular dermis were observed, as well as quantitative reduction and reorganization of collagen, in addition to the decrease of the vascularization of the tissue through immunohistochemical analysis.
CONCLUSION: The basic principle of the whole physiological healing process is to reestablish local homeostasis, that is, excessively intensified steps that lead to severe clinical changes. When subcicatricial fat grafting associated with rigotomy was performed, qualitative and quantitative improvements of the tissue were verified in this study. Thus, it becomes evident that this procedure can complement the treatment of cicatricial pathologies.
Keywords: Skin grafting; Scar; Burns; Healing; Reconstructive surgical procedures.
Com o aumento da sobrevida na fase aguda do paciente grande queimado, a prevalência das sequelas cicatriciais também vem crescendo, o que incentiva cada vez mais o desenvolvimento de técnicas e procedimentos para seu tratamento.
O grande prejuízo estético-funcional de tais sequelas é resultado do desarranjo cicatricial induzido pelo trauma térmico1, no qual o estímulo desordenado das fases cicatriciais produz resultados catastróficos como cicatrizes hipertróficas e queloideanas que, na maioria das vezes, limitam a função articular.
Diversos estudos tentam quantificar por meios de escalas o impacto das cicatrizes na vida do indivíduo com sequela de queimadura, porém nota-se que a evidência para a maioria das recomendações para a terapia da cicatriz é limitada1.
Isso porque o processo cicatricial é um dos eventos mais complexos do metabolismo humano, envolvendo uma grande variedade de células e citocinas, além de sofrer influência de fatores externos.
Carrel, em 1910 (apud Guyton1), classificou este processo em três fases (inflamatória, proliferativa e maturativa), nos ajudando a compreender de maneira simplista a rotina da cicatrização, sendo que esta mesma ordem ocorre em todo processo cicatricial independentemente do tipo de tecido ou do tipo da agressão2. No entanto, dentro da complexidade de fatores que podem prejudicar o resultado final, sabe-se que a quantidade de tecido lesado e a gravidade da injúria são os principais elementos da desordem cicatricial3, presente em toda queimadura.
Como continuidade à resposta inflamatória inicial do processo de cicatrização, o tecido lesado inicia a angiogênese, fibroplasia e epitelização, ainda como meio de defesa ao ambiente externo. Esta fase é caracterizada pela formação do tecido de granulação composto por um leito capilar neoformado, fibroblastos, macrófagos e um arranjo de colágeno, fibronectina e ácido hialurônico.
Diversos estudos utilizando fatores de crescimento trabalham sobre a ideia de como modificar esta fase de proliferação, principalmente a fibroplasia, responsável pela maioria das cicatrizes patológicas pós-queimadura4. No entanto, pouco se conhece sobre os fatores que diminuem a resposta proliferativa cicatricial, ou seja, o que clinicamente poderia ser útil para reduzir a incidência de contraturas cicatriciais pós-queimadura5.
Ainda pensando no processo de formação das cicatrizes ditas patológicas, sabe-se que a continuidade do processo inflamatório, como nos casos de queimaduras, mantém o estímulo de ativação fibroblástica, criando assim um ambiente suturado em colágeno, cujo arranjo estrutural mostra-se diferente daquele apresentado na cicatrização normal6, o que resulta nas grandes contraturas cicatriciais.
Dentro deste conceito, dois fenômenos parecem ser cruciais para elucidação das reais alterações presentes nas contraturas: a organização das fibras de colágeno e o comportamento vascular cicatricial, espelho da resposta inflamatória prolongada4.
Logo, pensando em maneiras de oferecer ao tecido cicatricial algum fator que induza a remissão ou gere a reorganização tecidual local, foi proposto por Rigotti7, a partir de observações clínicas, que a lipoenxertia subcicatricial melhora a qualidade macroscópica e funcional das cicatrizes, ao gerar alterações estruturais durante as 14 semanas iniciais do processo de remodelamento cicatricial.
Vários trabalhos sobre procedimentos relacionados à lipoenxertia são constantemente publicados8,9, e neste caso a técnica proposta por estes autores7 chama atenção para o método de obtenção da gordura a ser enxertada, onde a não agressão física dos adipócitos é regra. Realiza-se lipoaspiração com cânulas de 12 orifícios e 2 mm de espessura, com pressão média de sucção de 250 mmHg, seguida da centrifugação em baixa rotação (15g) por 3 minutos. Para enxertia, utiliza-se a técnica de Rigottomy, na qual são realizadas diversas micropunções com agulha 18G sobre a área cicatricial para que crie um ambiente tridimensional de lipopreenchimento4 (Figura 1).
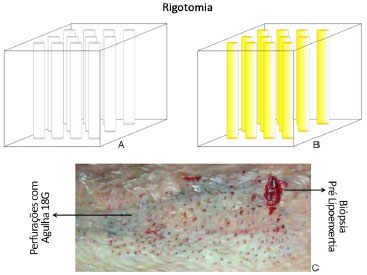
Figura 1. A: Tecido após punções com agulha 18G; B: Após a lipoenxertia subcicatricial; C: Aspecto "in vivo" da rigotomia.
A teoria proposta para melhoria da qualidade estrutural da cicatriz baseia-se na presença de produtos derivados de células-tronco4, no entanto, o conceito e a real contribuição das células-tronco ainda é um tema superficialmente explorado.
OBJETIVOS
Este trabalho tem por objetivo avaliar as reais alterações funcionais, microscópicas e imunohistológicas após a lipoenxertia subcicatricial em sequelas de queimadura, ao comparar o pré-operatório e o pós-operatório tardio (14 semanas) nos quesitos:
1. Avaliação estética e funcional da cicatriz pela Escala de Cicatrização de Vancouver10;
2. Análise microscópica quantitativa e qualitativa do colágeno cicatricial corado por hematoxilinaeosina e picrosirius;
3. Análise imunohistoquímica da vascularização cicatricial com anti-fator de crescimento derivado do endotélio vascular (antiVEGE).
MÉTODOS
Após aprovação pelo Comitê de Ética em Pesquisa (CAAE 33848214.9.0000.5430) e assinatura do Termo de Consentimento, foram selecionados, aleatoriamente, oito pacientes (quatro homens e quatro mulheres), com idade média de 35 anos (28-61 anos) do Ambulatório de Sequelas Cicatriciais do Departamento de Cirurgia Plástica da Faculdade de Medicina de Catanduva, SP, Brasil, todos vítimas de queimadura por álcool, com tempo médio pós-queimadura de 12 meses (10-14 meses), apresentando contratura cicatricial axilar e/ou cervical, e relatando disfunção articular pela sequela cutânea. Não apresenta conflito de interesse.
Todos foram submetidos à biópsia cutânea sobre a lesão, seguida de lipoenxertia subcicatricial associada à "Rigottomy", proposta por Rigotti 7, e descrita a seguir. Em seguida, após 14 semanas da lipoenxertia, foram submetidos a nova biópsia distando 2,5 cm da anterior, ainda sobre a cicatriz (Figura 2).
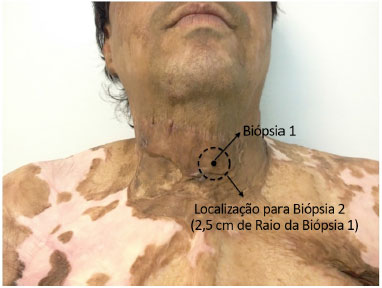
Figura 2. Padronização das biópsias cutâneas pré e pós-lipoenxertia.
Técnica Cirúrgica (Rigottomy)
Sob anestesia geral, foi obtido tecido adiposo (técnica super-úmida) do abdome inferior com cânulas de lipoaspiração de 12 orifícios e 2 mm com pressão de sucção média de 250 mmHg. O volume obtido foi de acordo com a superfície a ser enxertada. Ainda como descrito por Khouri et al.7, todo o volume foi submetido à centrifugação manual de baixa rotação (15 g) por 3 minutos, sem manipulação tecidual após a centrifugação como preconizado por Coleman11.
A área cicatricial a ser lipoenxertada foi submetida a microperfurações com agulha 18G até o nível hipodérmico, com distância média de 5 mm entre cada orifício. Com uma cânula de infiltração de 2 mm, foi realizada a distribuição retrógrada e linear do enxerto sob o tecido cicatricial. Após o procedimento, realiza-se a microporagem local para estabilização do enxerto subcutâneo.
Para análise comparativa, foram criados dois grupos: pré e pós-lipoenxertia, com intervalo de 14 semanas e em cada momento todos os pacientes foram avaliados para os seguintes critérios:
1. Avaliação estética e funcional da cicatriz pela Escala de Cicatrização de Vancouver (Tabela 1), na qual as menores pontuações representam a melhor qualidade cicatricial.
2. Análise microscópica quantitativa e qualitativa do colágeno cicatricial, em que todos os pacientes foram submetidos à biópsia em fuso da cicatriz até o nível hipodérmico antes e após 14 semanas da lipoenxertia, com distância máxima entre os locais de biópsia de 2,5 cm (Figura 2).O material foi corado com hematoxilina-eosina e picrosirius, sendo analisado em microscópico com e sem luz polarizada (Layca®), o que permitiu averiguar a organização do colágeno local. Com auxílio do software Prisma Graph Pad®, realizou-se a quantificação do colágeno pela densidade e pelo espectro de luz, sendo que, sob luz polarizada e corado pelo picrosirius, o colágeno normal (organizado) mostra-se com coloração amarelo-esverdeada, já o tecido fibrótico com colágeno desorganizado, mostra-se vermelho-alaranjado.
3. Análise imunohistoquímica da vascularização cicatricial, na qual o mesmo tecido utilizado na avaliação anterior foi agora marcado com anticorpo antiVEGF e analisado sobre luz polarizada. A análise do VEGF pelo software Prisma Graph Pad® permitiu quantificar a neovascularização tecidual dos dois momentos. Lembrando que todo processo de indução vascular a partir do VEGF traduz algum grau de inflação local, ou seja, quanto maior o índice de neovascularização, maior é a resposta inflamatória tecidual1.Foram utilizadas como testes estatísticos: Teste t e Wilcoxon.
RESULTADOS
A avaliação dos pacientes nos dois momentos, com intervalo de 14 semanas, apresentou resultados significativos para a melhora tecidual induzida pela lipoenxertia. Ao utilizarmos a escala de Vancouver, verificou-se a redução da pontuação em todos os casos. Ou seja, melhora estético-funcional das cicatrizes após a lipoenxertia e Rigotomia (Figura 3).
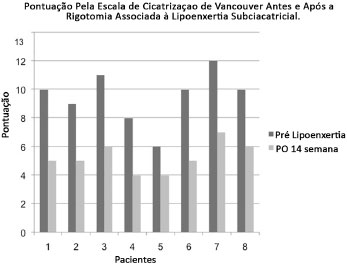
Figura 3. Evolução da pontuação na Escala de Vancouver dos pacientes. Evidência da melhora estético-funcional das cicatrizes após a lipoenxertia.
Quanto à avaliação microscópica pela hematoxilinaeosina (Figura 4) e pelo Picrosirius, pode-se verificar a melhora estrutural do tecido submetido à lipoenxertia, tanto pela redefinição entre derme papilar e reticular quanto pela reorganização e redução quantitativa (p < 0,05) do colágeno cicatricial avaliado pela interpretação dos espectros de luz no software Prima Graph Pad® (Figura 5).
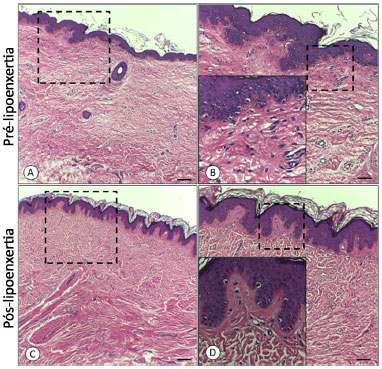
Figura 4. A: Pré-lipoenxertia; B: Pré-lipoenxertia com magnificação na transição dermo-epidérmica; C: Pós-lipoenxertia; D: Pós-lipoenxertia com magnificação na transição dermo-epidérmica.
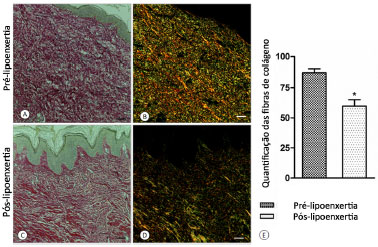
Figura 5. A: Pré-lipoenxertia; B: Pré-lipoenxertia sob luz polarizada; C: Pós-lipoenxertia; D: Pós-lipoenxertia sob luz polarizada; E: Grafico de quantificação do Colágeno.
No quesito neovascularização, houve redução do processo induzido pelo VEGF entre os dois períodos, com redução da vascularização tecidual no tecido lipoenxertado (p < 0,05) (Figura 6) quando avaliado comparativamente pela imunohistoquímica em conjunto ao software Prima Graph Pad®.
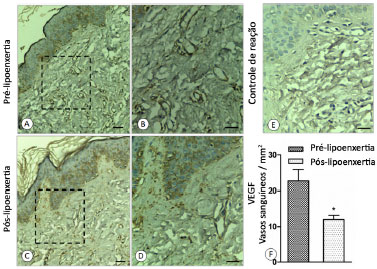
Figura 6. A: Pré-lipoenxertia; B: Pré-lipoenxertia com magnificação; C: Pós-lipoenxertia; D: Pós-lipoenxertia com magnificação; E: Controle de Reação; F: Gráfico da concentração de VEGF.
VEGF: fator de crescimento derivado do endotélio vascular.
DISCUSSÃO
Todo processo cicatricial baseia-se na deposição e remodelação das fibras de colágeno. Tudo é iniciado por uma resposta inflamatória que, de acordo com a área de lesão e a gravidade do agente, pode-se intensificar ou não essas etapas1.
Alguns fenômenos cicatriciais, como a neovascularização, dependem dos fatores de indução da resposta inflamatória, sendo estes mais intensos quando a inflamação persiste ou é inicialmente muito grande2. Logo, cicatrizes com uma intensa fase inflamatória, como no caso das queimaduras, apresentam uma rica rede neovascular, constantemente induzida pelo VEGF (fator de crescimento derivado do endotélio vascular) e, uma maneira de quantificar o status inflamatório do tecido cicatricial, seria avaliar o seu grau de neovascularização.
No caso das cicatrizes patológicas (sequelas de queimadura) a intensa neovascularização tecidual, demonstrada neste estudo, confirma o grande potencial inflamatório deste tecido, sendo que a introdução de células adiposas e seus resíduos no interstício cicatricial promoveu uma redução significativa da resposta inflamatória e, consequentemente, na vascularização patológica local (p < 0,05). Sendo que a relação entre neovascularização e processo inflamatório é direta; pode-se supor que tal decréscimo vascular após a lipoenxertia esteja relacionado à redução do processo inflamatório crônico local.
Em consequência a isto, pode-se também observar a reorganização estrutural do tecido cicatricial pelo realinhamento e redução quantitativa das fibras de colágeno, o que se traduz clinicamente na melhora funcional e macroscópica do tecido, permitindo liberdade de movimento articular, antes restrito pela contratura. Além disso, a reorganização induzida pela lipoenxertia permitiu um novo delineamento entre a derme papilar e a reticular, antes perdido.
No que se refere ao agente indutor da reorganização e redução inflamatória presente no tecido adiposo, novos estudos de ordem molecular e genética precisam ser realizados. No entanto, a simples justificativa da presença de células-tronco no tecido adiposo precisa ser cuidadosamente avaliada e redefinidos alguns conceitos básicos sobre o assunto. Isso para que não sejam subestimados outros fatores de menor complexidade como possíveis responsáveis pelo estímulo patológico que desencadeia as grandes e disfuncionais sequelas cicatriciais.
CONCLUSÃO
O princípio básico de todo processo cicatricial fisiológico é restabelecer a homeostasia local, ou seja, as etapas exageradamente intensificadas levam a alterações clínicas catastróficas.
No caso das sequelas cicatriciais de queimadura o desenvolvimento de terapias para melhoria ou resolução deste processo traz ao paciente um ganho funcional, psicológico e econômico, uma vez que restabelece suas atividades laborais.
Ao realizar a lipoenxertia subcicatricial, foi provado neste estudo a melhora qualitativa e quantitativa do tecido cicatricial, uma vez que pode-se avaliar microscopicamente a redução do processo inflamatório, a reorganização estrutural da cicatriz pela definição entre derme papilar e reticular, além da redução quantitativa da neovascularização e do colágeno local (p < 0,05).
Logo, conclui-se que o processo de lipoenxertia subcicatricial associada à técnica de Rigottomy4 altera positivamente a microestrutura cicatricial, apresentando benefícios macro e microscópicos. Sendo assim, torna-se evidente o futuro promissor da lipoenxertia autóloga para a complementação terapêutica das patologias cicatriciais.
AGRADECIMENTOS
À Disciplina de Cirurgia Plástica da Faculdade de Medicina de Catanduva, regida pelo Prof. Dr. Manoel Alves Vidal, que proporcionou toda a estrutura para realização deste trabalho, além da disciplina de Histologia/Patologia, representada pela Prof. Dra. Ana Paula Girol, que nunca se absteve do compromisso em disponibilizar seus conhecimentos para a conclusão deste estudo.
COLABORAÇÕES
AMLAF Análise e/ou interpretação dos dados; aprovação final do manuscrito; concepção e desenho do estudo; realização das operações e/ou experimentos; redação do manuscrito ou revisão crítica de seu conteúdo.
BPV Concepção e desenho do estudo.
MAV Análise e/ou interpretação dos dados; aprovação final do manuscrito; concepção e desenho do estudo; realização das operações e/ou experimentos; redação do manuscrito ou revisão crítica de seu conteúdo.
APG Análise e/ou interpretação dos dados; análise estatística; realização das operações e/ou experimentos.
HRS Análise e/ou interpretação dos dados; realização das operações e/ou experimentos.
MG Realização das operações e/ou experimentos.
REFERÊNCIAS
1. Carrel A. The treatment of wounds. JAMA. 1910; 55:2148. Apud Guyton AC. Guyton and Hall Textbook of Medical Physiology. 10th ed. Philadelphia: Saunders; 2000. p. 385-387.
2. Del Vecchio D, Rohrich RJ. A classification of clinical fat grafting: different problems, different solutions. Plast Reconstr Surg. 2012;130(3):511-22.
3. Durani P, McGrouther DA, Ferguson MW. Current scales for assessing human scarring: a review. J Plast Reconstr Aesthet Surg. 2009;62(6):713-20.
4. Sterodimas A, de Faria J, Nicaretta B, Boriani F. Autologous fat transplantation versus adipose-derived stem cell-enriched lipografts: a study. Aesthet Surg J. 2011;31(6):682-93.
5. Lu F, Li J, Gao J, Ogawa R, Ou C, Yang B, et al. Improvement of the survival of human autologous fat transplantation by using VEGF-transfected adipose-derived stem cells. Plast Reconstr Surg. 2009;124(5):1437-46.
6. Aiba-Kojima E, Tsuno NH, Inoue K, Matsumoto D, Shigeura T, Sato T, et al. Characterization of wound drainage fluids as a source of soluble factors associated with wound healing: comparison with platelet-rich plasma and potential use in cell culture. Wound Repair Regen. 2007;15(4):511-20.
7. Khouri RK, Rigotti G, Cardoso E, Khouri RK Jr, Biggs TM. Megavolume autologous fat transfer: part II. Practice and techniques. Plast Reconstr Surg. 2014;133(6):1369-77.
8. Bersou Júnior A. Lipoenxertia: técnica expansiva. Rev Bras Cir Plást. 2008;23(2):89-97.
9. Oliveira Neto FV. Enxerto de gordura humana em ratos: Estudo comparativo de diferentes preparos da gordura. Rev Bras Cir Plást. 2011;26(3 Suppl. 1):5.
10. Baryza MJ, Baryza GA. The Vancouver Scar Scale: an administration tool and its interrater reliability. J Burn Care Rehabil. 1995;16(5):535-8.
11. Coleman SR. Structural fat grafting: more than a permanent filler. Plast Reconstr Surg. 2006;118(Suppl):108S-20S.
Faculdade de Medicina de Catanduva, Catanduva, SP, Brasil
Instituição: Faculdade de Medicina de Catanduva, Catanduva, SP, Brasil.
Autor correspondente:
Auro Marcos Levy de Andrade Filho
Rua Jesus Blanco Nunes, 43 - Santa Marta
São Carlos, SP, Brasil CEP 13564-270
E-mail: aurinhu@yahoo.com.br
Artigo submetido: 17/5/2015.
Artigo aceito: 6/8/2016.
Conflitos de interesse: não há.



 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter