
Articles - Year 1999 - Volume 14 -
Doença de Meige (Linfedema Precoce) - Relato de Caso e Revisão de Literatura
Doença de Meige (Linfedema Precoce) - Relato de Caso e Revisão de Literatura
RESUMO
Linfedema primário é um distúrbio causado por edema persistente, principalmente nas extremidades e com predominância em mulheres. O diagnóstico pode ser feito através da história clínica, exame físico e com exames complementares como linfangiografia, venografia e linfocintilografia. As complicações mais freqüentes são ataques recorrentes de celulite e linfangite, e raramente linfangiosarcoma. O tratamento do linfedema primário baseia-se em medidas de apoio, elevação da extremidade, atividade física, compressão elástica; entretanto, na falência do tratamento clínico, está indicada a cirurgia. Descreve-se o caso de uma paciente de 29 anos, com quadro de linfedema primário, que apresentava alterações no fluxo do sistema linfático na investigação, sendo submetida ao procedimento de Charles associado à enxertia precoce. A literatura foi revisada.
Palavras-chave: Doença de Meige; linfedema precoce; procedimento de Charles; enxertia precoce de pele parcial
ABSTRACT
Primary lymphedema is a disorder caused bypersistent edema, mainly of extremities and predominating in women. Diagnosis may be made through clinical history, physical examination and supplementary examinations such as lymphangiography, venography and lymphoscintscanning. More frequent complications are recurrent cellulitis and lymphangitis, and rarely lymphangiosarcoma attacks. Treatment ofprimary lymphedema is based on support measures, extremity raising, physical activity, elastic compression; howeven when failure of clinical treatment occurs, surgery is indicated. The case of a 29-year patient with primary lymphedema presenting changes in lymphatic system flow at investigation and being submitted to Charles's procedure associated to early grafting is described. Literature was reviewed.
Keywords: Meige's disease; early lymphedema; Charles's procedure; early partial skin graft
Linfedema é uma síndrome caracterizada pelo acúmulo de fluido hiperprotéico na derme e tela subcutânea, porém não nos tecidos profundos da parede muscular. A etiologia inclui anormalidades congênitas no desenvolvimento do sistema linfático ou secundário; a obstrução, destruição ou mau funcionamento da rede linfática. Dentre as causas mais comuns estão a infecção, estado pós-flebítico com estase venosa, infiltração de tecidos locais ou linfonodos regionais por células malignas e pós-linfadenectomia, com ou sem radioterapia(1,2,3).
CLASSIFICAÇÃO E APRESENTAÇÃO CLÍNICA
O linfedema divide-se em primário e secundário. O linfedema primário ou idiopático pode ser subdividido em forma congênita (Doença de Milroy)(4), presente no nascimento; linfedema precoce (Doença de Meige)(5), a qual aparece geralmente dos 10 aos 35 anos, e linfedema tardio, que aparece após os 35 anos. Linfedema precoce compreende aproximadamente 80% dos casos de linfedema primário, com predominância em mulheres. Quando vários membros da mesma família têm linfedema congênito, esta patologia tem sido chamada de Doença de Nonne-Milroy-Meige(6). A idade de surgimento e a severidade tendem a ser similares em uma família(7, 8, 9).
A apresentação clínica do tipo familiar não é diferente da expressão não familiar. Os pacientes, em sua maioria, são mulheres (75%). Os locais mais freqüentemente envolvidos são as pernas, mas os braços, a genitália e a face podem ser afetados. O edema aparece nos calcanhares e gradualmente estende-se em direção superior. As extremidades inferiores podem eventualmente ser acometidas. A ocorrência de trauma tem sido descrita como agente desencadeante.
O edema é inicialmente mole e desaparece durante o repouso, mas torna-se firme com o passar do tempo devido à complicação da fibrose reativa. Temperatura elevada, menstruação e gestação podem acentuar o edema. Alterações da pele por linfedema, trauma, fissura e epidermofitose permitem a entrada de bactérias, especialmente estreptococos hemolíticos e menos freqüentemente estafilococos, causando linfangite e celulite recorrentes.
A patogênese do linfedema ainda é desconhecida. Independente da causa primária do linfedema (malformação ou obstrução), o edema ocorre quando a filtração capilar excede a reabsorção linfática e venosa. A fase inicial do linfedema é reversível. Uma vez ocorrida a fibrose tecidual, as mudanças são irreversíveis. Infecções e neoplasias são as maiores complicações do linfedema. O edema rico em proteínas serve como um excelente meio de crescimento bacteriano. Esses pacientes irão inevitavelmente desenvolver celulite e linfangite. Aproximadamente 25% dos pacientes vivencia inevitáveis episódios de linfangite. Portanto, terapia agressiva de longa duração, com baixas doses de antibiótico oral para infecções por estafilococos e estreptococos, pode ser benéfica.
DIAGNÓSTICO
O diagnóstico do linfedema é principalmente clínico, baseado na história, exame físico e exclusão de outras possibilidades. Usualmente a extremidade envolvida é dolorosa, sem nenhuma capacidade funcional, edemaciada, fria e com coloração azulada.
Vários métodos diagnósticos podem ser úteis: linfangiografia, a qual não é realizada rotineiramente por causa de dificuldades técnicas e complicações, e linfocintilografia, que é segura, confiável e tornou-se o método de escolha para visualização e avaliação da função linfática. Outros métodos diagnósticos incluem ultra-sonografia doppler, tomografia axial computadorizada e ressonância magnética nuclear(9, 10, 11, 12, 13, 14, 15).
DIAGNÓSTICO DIFERENCIAL
O diagnóstico diferencial de linfedema inclui as formas comuns de edema bilateral (como nefrose, insuficiência cardíaca congestiva, edema cíclico ou idiopático, estados de hipoproteinemia e mixedema) e condições edematosas unilaterais (como insuficiência venosa, angiodermatite e lipedema). O achado clínico de edema não depressível, firme, favorece a origem linfedematosa, mas uma biópsia associada a linfangiograma e venograma pode ser necessária para fazer o diagnóstico definitivo(7).
COMPLICAÇÕES
As principais complicações do linfedema são episódios recorrentes de celulite e linfangite. Uma rara complicação é o desenvolvimento de linfangiossarcoma, que pode surgir a partir do linfedema congênito(7).
TRATAMENTO
Linfedema é uma condição incurável em termos de total desaparecimento do edema e restituição do contorno da extremidade. A maioria dos pacientes com linfedema pode ser satisfatoriamente tratada clinicamente com apoio mecânico ou medicações, ou ambos.
O tratamento do linfedema tem como objetivo manter os tecidos livres de edema para prevenir fibrose e infecções bacterianas recorrentes. Perda de peso, elevação freqüente da extremidade envolvida, uso de malha elástica graduada, fisioterapia, diuréticos e uma dieta pobre em sal são medidas terapêuticas de rotina. A bomba de compressão pneumática externa ou compressão seqüencial intermitente seguida do uso diário de malhas elásticas graduadas na extremidade acometida podem ser úteis na redução do linfedema. A epidermofitose deve ser tratada vigorosamente e controlada. Profilaxia antibiótica intermitente de longa duração é recomendada para linfangite recorrente.
Os fatores que agravam o edema incluem uso excessivo do membro, calor local, aumento da temperatura ambiente e ferimentos por objetos pontiagudos. A ulceração é incomum e usualmente segue um trauma local.
Tratamento Cirúrgico
O tratamento cirúrgico é a área de maior controvérsia. Charles propôs uma das primeiras técnicas excisionais em 1912, a qual consiste na retirada da pele e tela subcutânea até a fáscia muscular, apresentando resultados relativamente bons, reduzindo o tamanho da extremidade, deixando entretanto uma cicatriz residual e uma aparência pós-operatória desgraciosa(7, 10, 17). Thompson (1960) desenvolveu o procedimento do retalho dérmico embricado para melhorar a drenagem linfática dos tecidos subcutâneos para os troncos linfáticos profundos. Inicialmente os resultados foram encorajadores, mas tardiamente investigadores demonstraram que o sucesso da operação era causado somente pela remoção do tecido linfático(18). Goldsmith e colaboradores desenvolveram uma técnica de transposição de omento rico em tecido linfático para drenar a extremidade envolvida. Os resultados desta operação têm sido pobres(19). Atualmente tem sido utilizada microcirurgia para criar anastomoses linfático-venosas na tentativa de desviar as obstruções do sistema linfático(17).
O procedimento cirúrgico é recomendado para pacientes com edema não controlado, deformidade excessiva e diminuição da mobilidade devido ao tamanho da extremidade. O paciente precisa ser hospitalizado, devendo manter a extremidade elevada por vários dias a fim de eliminar todo o edema residual antes da operação. Se necessário, uma bomba pneumática pode ser usada. O tratamento cirúrgico não é indicado para crianças com menos de 2 anos, pois ocasionalmente o edema poderá diminuir com o início da deambulação. Os resultados do tratamento cirúrgico em extremidades são menos satisfatórios que o esperado, entretanto, em operações genitais, o tratamento cirúrgico tem obtido bons resultados(3).
Em resumo, a cirurgia de extremidades deve ser utilizada como último recurso quando as medidas conservadoras falharem. Cirurgia precoce em crianças e adolescentes deve ser evitada por causa da alta variabilidade de curso da doença. Se a cirurgia for indicada, o paciente deverá ser avisado de que há somente 30% de sucesso nesse procedimento e de que as complicações, especificamente cosméticas, são freqüentes. Um fato desencorajador permanece: nenhum procedimento cura o linfedema(17, 8).
RELATO DE CASO
Paciente do sexo feminino, de 29 anos, natural de Curitiba-PR, com quadro de trombose venosa superficial em membro inferior esquerdo, há 11 anos, associado a quadro de erisipela. Submetida a tratamento clínico com venodilatador, antiinflamatórios e antibióticos, obteve melhora relativa, porém com persistência do edema no tornozelo. Um ano após esse quadro, foi realizada uma flebografia, sem anormalidades. Há 9 anos apresentou edema importante de raiz de coxa esquerda associado a quadros recorrentes de erisipela. Nesse período utilizou meia elástica de alta compressão e compressor pneumático externo, obtendo redução do edema.
Na primeira gestação, há 4 anos, apresentou aumento de volume do membro afetado (Fig. 1). No ano seguinte, foi submetida a cirurgia de "shunt" linfovenoso em região inguinal, com diminuição do volume da coxa. Em novembro do mesmo ano, realizou cirurgia com retalho embricado (Thompson - Fig. 2), tendo como resultado piora do quadro clínico e incapacidade funcional, acentuada após a segunda gestação, dois anos após a primeira. Há 1 ano realizou linfocintilografia de membros inferiores, que demonstrou a ausência de vasos linfáticos no membro inferior esquerdo, submetendo-se em seguida à cirurgia de Charles (Figs. 4, 6 e 7), exceto em área de articulação de joelho e raiz de coxa, com a finalidade de preservar a pele sadia. A peça cirúrgica pesava aproximadamente 40 kg (Fig. 5). Foi realizada a enxertia imediata de pele parcial, retirada da peça com faca de Blair (Fig. 3) e preparada com expansor de Tanner (Fig. 8).
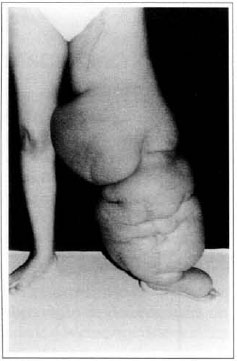
Fig. 1- Linfedema primário.
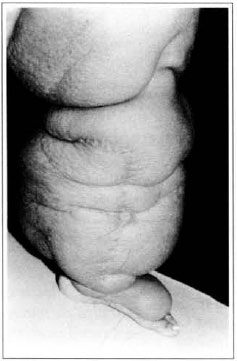
Fig. 2 -Aspecto "peau d'orange" e cicatriz de cirurgia de Thompson.
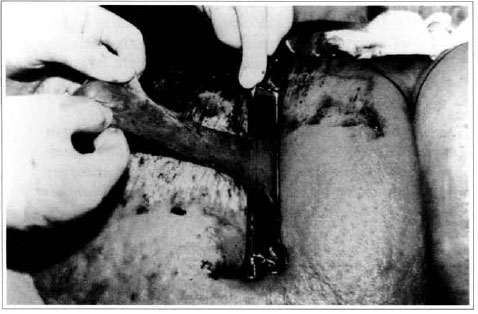
Fig. 3 - Retirada de enxerto de pele parcial.
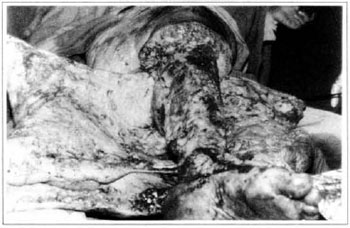
Fig. 4 - Cirurgia de Charles.
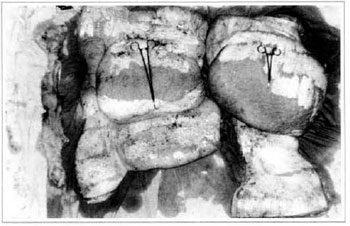
Fig. 5 - Peça cirúrgica.
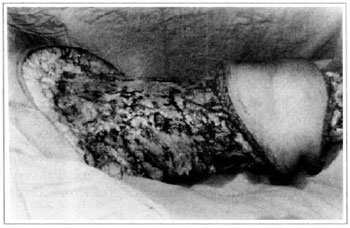
Fig. 6 - Cirurgia de Charles - transoperatório.
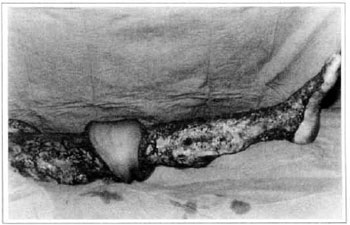
Fig. 7 - Cirurgia de Charles - transoperatório.
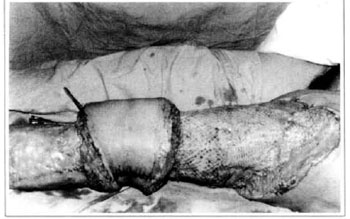
Fig. 8 - Aspecto imediato de enxerto de pele - "mesh-graft" na coxa.
A paciente permaneceu internada por um período de 30 dias, sendo submetida a curativos oclusivos, a cada 2 dias, com polvidine tópico, solução salina isotônica, rayon vaselinado e rifamicina tópica, permanecendo no quarto com o membro inferior elevado. Antibioticoterapia sistêmica também foi realizada. A paciente foi submetida a fisioterapia motora por 20 dias após o procedimento, recebendo alta deambulando, com enxerto integrado (Figs. 9 e 10) e retorno agendado para lipoaspiração em articulação de joelho. Após 60 dias, a paciente foi submetida a novo procedimento cirúrgico para diminuir diâmetro da pele e tela subcutânea em região de articulação de joelho associado a lipoaspiração (Fig. 11), utilizando meia elástica na seqüência. Ela permaneceu com quadro estável, com o volume do membro inferior mantido por um período de 3 meses. Provavelmente pelo fato de a paciente não utilizar meia elástica, houve recidiva do edema em região de articulação de joelho, tendo-se optado pela ressecção de pele e tela subcutânea e enxerto de pele parcial imediato. Após 6 meses desse último procedimento, a paciente encontra-se estável, sem recidivas ou edema residual (Figs. 12 e 13), necessitando apenas de correção de linfedema de raiz de coxa.
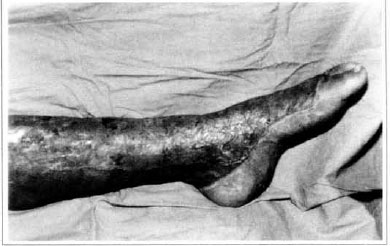
Fig. 9 - Enxerto integrado.
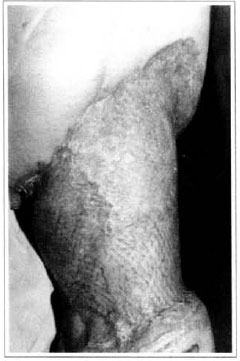
Fig. 1O - Aspecto final do "mesh-graft" - volume residual em coxa.
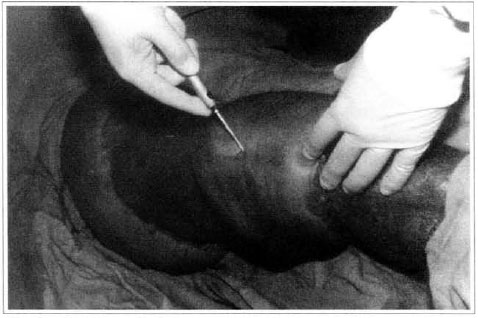
Fig. 11 - Lipoaspiração de joelho.
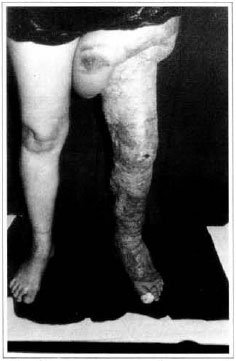
Fig. 12 - Aspecto pós-operatório tardio, 6 meses - vista anterior.
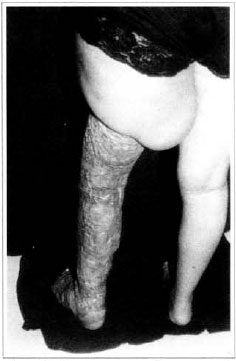
Fig. 13 - Aspecto pós-operatório tardio, 6 meses - vista posterior.
BIBLIOGRAFIA
1. ARAÚJO JA, CURBELO JG. Effective management of marked lymphedema of the leg. Int. J. Derm. 1997; 36:389-392.
2. MORTIMER P, REGNARD C. Lymphostatic disorders. Br. J. Surg. 1986; 293:347-348.
3. MOREY AF, MENG MV, McANINCH JW. Skin graft reconstruction of chronic genital lymphedema. Urology. 1997; 50(3):423-6.
4. MILROY WF. Chronic hereditary edema: Milroy's disease. JAMA. 1928; 91:1172-1174.
5. MEIGE H. Dystrophie oedémateuse héréditaire. Presse Med. 1898; 2:341-343.
6. NONNE M. Vier Fälle von Elephantiasis congenita hereditaria. Arch. Pathol. Anat. Physiol. 1891; 125:189-196.
7. KINMONTH JB. Primary lymphedema of the lower limb. Proc. R. Soc. Med. 1965; 58:1021-1025.
8. KINMONTH JB, TAYLOR GW, TRACY GD, MARSH JD. Primary lymphedema. Br. J. Surg. 1957; 65:3-9.
9. WOLFE JHN, KINMONTH JB. The prognosis of primary lymphedema of the lower limbs. Arch. Surg. 1981; 116:1157-1160.
10. HAREL L, AMIR J. Lymphedema praecox seen as isolated unilateral arm involvement: Case report and review of the literature. J. Pediat. 1997; 130:492-494.
11. PROBY CM, GANE JN. Investigation of the swollen limb with isotope lymphography. Br. J. Derm. 1990; 123:29-37.
12. GOUGH MH. Primary lymphoedema: Clinical and lymphangiographic studies. Br. J. Surg. 1966; 53:917-925.
13. DUEWEL S, HAGSPIEL KD. Swollen lower extremity: Role of MR Imaging. Radiology. 1992; 184:227-231.
14. WEISSLEDER H, WEISSLEDER R. Lymphedema: Evaluation of qualitative and quantitative lymphoscintigraphy in 238 patients. Radiology. 1988; 167:729-735.
15. HARWOOD CA, BULL RH, EVANS J, MORTIMER PS. Lymphatic and venous function in lipoedema. Br. J. Surg. 1996; 134:1-6.
16. CHARLES H. A system of treatment. Latham & English, 1912. Vol 1, p. 123-147.
17. SMELTZER DM, STICKLER GB, SCHIRGER A. Primary lymphedema in children and adolescents: A follow-up study and review. Pediatrics. 1985; 76:206-217.
18. THOMPSON N. Ibid. 1962; 2:1566.
19. GOLDSMITH HS, DE LOS SANTOS R, BEATTIE EJ. Relief of chronic lymphedema by omental transposition. Ann. Surg. 1967; 166:573-585.
I - Médico Residente do Serviço de Cirurgia Plástica.
II - Membro Titular da SBCP. Serviço de Cirurgia Plástica e Queimados do Hospital Evangélico de Curitiba.
III - Cirurgião vascular - Departamento de Cirurgia Vascular - Hospital Evangélico de Curitiba.
IV - Estudante de Medicina.
Endereço para correspondência:
Ronaldo Roesler
R. Aristides Athayde Jr., 560 - apto. 171
Curitiba - PR 80730-370
Fone: (41) 336-8178


 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter