
Original Article - Year 2026 - Volume 41Issue 1
Integração de novas terapias biológicas ao Sistema Único de Saúde: Avaliação logística e primeiras aplicações clínicas do transplante legalizado de membrana amniótica
Integration of New Biological Therapies into the Brazilian Unified Health System: Logistics Assessment and First Clinical Applications of Legalized Amniotic Membrane Transplantation
RESUMO
Introdução A membrana amniótica humana (MA) possui propriedades imunomoduladoras e regenerativas que a tornam valiosa no tratamento de queimaduras e lesões cutâneas complexas. No Brasil, a Portaria n° 8.244, de setembro de 2025, regulamentou seu processamento e uso clínico por bancos de multitecidos.
Objetivo Apresentar os resultados operacionais iniciais da implementação deste novo recurso terapêutico em um banco de tecidos credenciado.
Materiais e Métodos Trata-se de um estudo descritivo, do tipo nota prévia, que avaliou o período de 07 de outubro a 26 de novembro de 2025, ao longo de 50 dias. Os dados operacionais (captação, processamento, distribuição) e clínicos (primeiros transplantes) foram analisados. O processamento envolveu triagem rigorosa de doadoras, tratamento antibiótico, manipulação em sala limpa com fluxo laminar com qualificação 5 da Organização Internacional de Normalização (ISO) e controle de qualidade microbiológico e sorológico. O tecido foi liberado após resultados negativos consistentes.
Resultados O Banco de Tecidos Dr. Roberto Corrêa Chem (BTDRCC) captou 13 MA e alcançou 100% de conformidade microbiológica e sorológica. O volume total liberado foi de 4.157 cm2 (60% distribuídos), com um intervalo médio de 12,5 dias entre captação e liberação. O primeiro transplante legalizado de MA no Brasil foi realizado no período avaliado.
Conclusão Os resultados preliminares validam a viabilidade operacional e a segurança do protocolo estabelecido pelo BTDRCC, garantindo 100% de conformidade microbiológica e liberação rápida de tecido. Estes dados estabelecem a base para futuras investigações sobre os desfechos clínicos e a análise de custos do uso da MA no cenário brasileiro.
Palavras-chave: membrana amniótica; transplantes; bancos de tecidos; queimaduras; enxerto
ABSTRACT
Introduction The human amniotic membrane (AM) possesses immunomodulatory and regenerative properties, making it valuable in the treatment of burns and complex skin lesions. In Brazil, Ordinance No. 8,244, issued in September 2025, regulates the processing and clinical use of AM by multi-tissue banks.
Objective To present the initial operational results from implementing this new therapeutic resource in an accredited tissue bank.
Materials and Methods This descriptive study, a preliminary note, evaluated the period from October 7 to November 26, 2025, spanning 50 days. We analyzed both operational (recruitment, processing, and distribution) and clinical data (initial transplants). The processing involved thorough donor screening, antibiotic treatment, handling in a cleanroom with International Organization for Standardization (ISO) 5 laminar flow hood qualification, and microbiological and serological quality control. Tissue release occurred only after consistently negative test results.
Results Dr. Roberto Corrêa Chem Tissue Bank (BTDRCC) harvested 13 AMs and achieved 100% compliance with microbiological and serological standards. The total volume released was 4,157 cm2 (60% distribution), with an average interval from harvesting to release of 12.5 days. The first legally authorized AM transplant in Brazil occurred during this period.
Conclusion Preliminary results validate the operational feasibility and safety of the protocol established by BTDRCC, ensuring 100% microbiological compliance and rapid tissue release. These data form the basis for future investigations into the clinical outcomes and cost analysis of AM use in the Brazilian setting.
Keywords: amniotic membrane; transplants; tissue banks; burns; graft
Introdução
A membrana amniótica (MA), estrutura avascular derivada da placenta, tem sido amplamente estudada devido às suas propriedades imunobiológicas e regenerativas. Sua composição inclui matriz extracelular rica em colágeno tipo I, III, IV, Ve VII, além de fibronectina, laminina e proteoglicanos. Os componentes a conferem características anti-inflamatórias, imunomoduladoras, antimicrobianas e epitelizantes.1 A MA também apresenta células epiteliais e mesenquimais com perfil de pluripotência e baixa imunogenicidade permite seu uso alogênico com risco mínimo de rejeição. Estudos clínicos e experimentais demonstram que a MA acelera a reepitelização, reduz a dor, minimiza a formação de cicatrizes hipertróficas e atua como barreira biológica temporária em feridas complexas, especialmente em queimaduras e lesões cutâneas extensas.2
No Brasil, até setembro de 2025, seu uso clínico estava restrito a protocolos experimentais ou importação sob demanda. A publicação da Portaria GM/MS n° 8.244, em 25 de setembro de 2025, viabilizou a regulamentação do processamento e aplicação clínica da MA por bancos de multitecidos.3 Esta portaria, ao incluir explicitamente o transplante de MA na tabela de procedimentos do Sistema Único de Saúde (SUS), viabilizou a atuação legalizada e não experimental das instituições credenciadas no Sistema Nacional de Transplantes. Esta regulamentação é um fator determinante, pois eleva essa terapia como um padrão de tratamento estabelecido, com protocolos definidos de captação e controle de qualidade.
Diante da nova regulamentação, o Banco de Tecidos Dr. Roberto Corrêa Chem (BTDRCC), da Santa Casa de Porto Alegre, adaptou sua infraestrutura para incorporar o processamento da MA. O presente artigo visa apresentar os resultados operacionais iniciais desta implementação, avaliando o impacto logístico e clínico imediato deste novo recurso terapêutico.
Materiais e Métodos
Este é um estudo descritivo, caracterizado como nota prévia, que abrange o período de 7 de outubro de 2025 a 26 de novembro de 2025, ao longo de 50 dias. Os dados analisados são de natureza operacional (captação, processamento, controle de qualidade, distribuição) e clínica (registro dos primeiros transplantes). Este estudo está em conformidade com parecer aprovado pelo Comitê de Ética em Pesquisa da instituição, com o CAAE: 59854922.5.0000.5335. O termo de consentimento livre e esclarecido foi assinado pelas doadoras de MA antes do parto.
Foram definidos critérios de inclusão: gestantes entre 18 e 35 anos, submetidas a cesariana eletiva, idade gestacional de 34 a 40 semanas, sorologias negativas, ausência de intercorrências obstétricas e de comorbidades infecciosas ou autoimunes ativas.
Os critérios de exclusão foram ruptura prematura de membranas maior que 12 horas, trabalho de parto superior a 24 horas, presença de corioamnionite, endometrite, febre ou sinais de infecção, uso de drogas ilícitas, histórico de neoplasias hematológicas, doenças autoimunes sistêmicas, infecções congênitas suspeitas ou confirmadas, sofrimento fetal e qualquer alteração placentária que comprometesse a integridade do tecido.
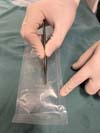
Todo o processo de captação de membrana amniótica foi realizado em sala de centro cirúrgico. Salas limpas, degermação de mãos e antebraços, paramentação cirúrgica e utilização de materiais estéreis fizeram parte das rotinas da captação do tecido. Após a cesariana, a membrana amniótica foi separada da placenta de forma asséptica, por meio de técnica digitiforme, sendo devidamente acondicionada e transportada ao Centro de Reabilitação Biovascular do BTDRCC mantida sob refrigeração (2–8° C). A ►Fig. 1 ilustra esses processos.
A continuidade do processamento da MA é dividida em três fases. Primeiro, no tratamento profilático da MA, acondicionada em solução contendo mescla de antibióticos e mantida sob refrigeração (2 a 8 °C) por um período mínimo de 8 horas. No dia seguinte ao tratamento antibiótico, a MA é submetida à 1ª fase do processamento, durante a qual o tecido é lavado com solução fisiológica estéril para a retirada do excesso de antibióticos e colocá-la em glicerol mais concentrado (95%). A 2ª fase consiste no aparo de bordas das lâminas de MA, embalagem e mensuração do tecido em cm2. A temperatura de armazenamento do tecido é de 2 a 8 °C.
Todos os materiais e instrumentos utilizados no processamento e que entraram em contato com a MA eram estéreis. A manipulação e exposição dos tecidos durante todo o processamento ocorreu em cabine de fluxo laminar com qualificação de ar 5 da Organização Internacional de Normalização (ISO).
A MA processada foi liberada e disponibilizada para uso terapêutico após avaliação macroscópica e testes microbiológicos negativos no tecido. Dessa forma, em cada fase do processamento foi realizada a coleta de fragmentos para a análise microbiológica. Os fragmentos foram colocados submersos em meios de cultura líquidos, inclusive tryptone soya broth (TSB) e tioglicolato, para propiciar o crescimento e recuperação de bactérias aeróbias, bactérias anaeróbias e fungos que possam estar presentes no tecido.
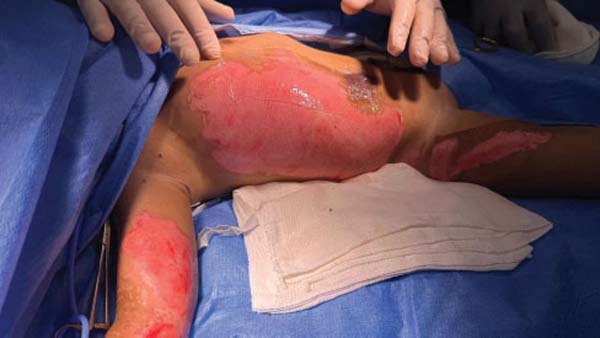
Adicionalmente, foi realizada a sorologia para citomegalovírus, toxoplasmose, vírus da imunodeficiência humana (HIV), vírus da hepatite C (HCV), vírus da hepatite B (HBV, HBc, HBsAG), vírus-T linfotrópico humano do tipo 1 (HTLV I e II), sífilis e doença de Chagas. Além da confirmação de HIV, HCV e HBV por análise molecular. A liberação do tecido para uso clínico foi condicionada à obtenção de resultados consistentemente negativos em todos os testes de contaminação e sorologia. Os tecidos liberados foram disponibilizados para distribuição através do Sistema Nacional de Transplantes. A ►Fig. 2 mostra como o biomaterial é disponibilizado para transplante.
Os dados de produção (captação, área processada, área distribuída) são de natureza quantitativa descritiva. Foram calculadas frequências absolutas e relativas para as variáveis categóricas (resultado do controle de qualidade) e estatísticas descritivas (média e amplitude) para o intervalo de tempo entre captação e liberação. Não foram aplicados testes de inferência estatística, dado o caráter inicial e descritivo da presente nota prévia.
Resultados
No período de 50 dias avaliado o BTDRCC demonstrou a capacidade operacional descrita na ►Tabela 1.
| Variável operacional | Índice |
|---|---|
| Captações de MA | 13 |
| Conformidade microbiológica e sorológica | 100% |
| Volume total de tecido liberado | 4.157 cm2 |
| Volume total de tecido distribuído | 2.485 cm2 |
| Porcentagem de distribuição | 60% |
| Intervalo médio captação-liberação | 12,5 dias |
| Instituições beneficiadas | 4 |
Abreviação: MA, membrana amniótica.
O BTDRCC alcançou um índice de 100% de conformidade microbiológica e sorológica nas 13 MA captadas. Este resultado foi obtido em um intervalo médio de 12,5 dias entre captação e liberação.
O volume total de tecido liberado totalizou 4.157 cm2, dos quais 2.485 foram distribuídos ativamente para quatro diferentes instituições hospitalares.
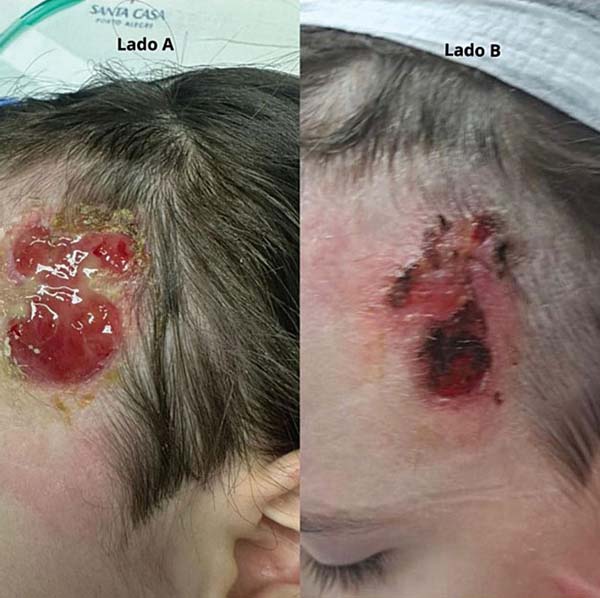
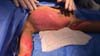
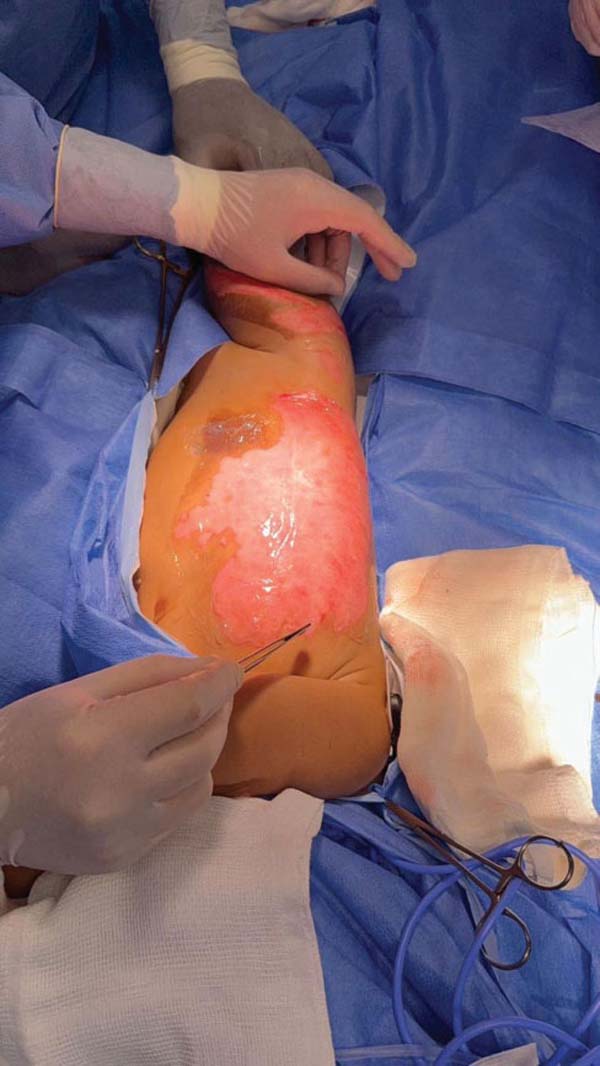
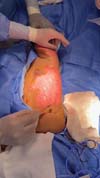
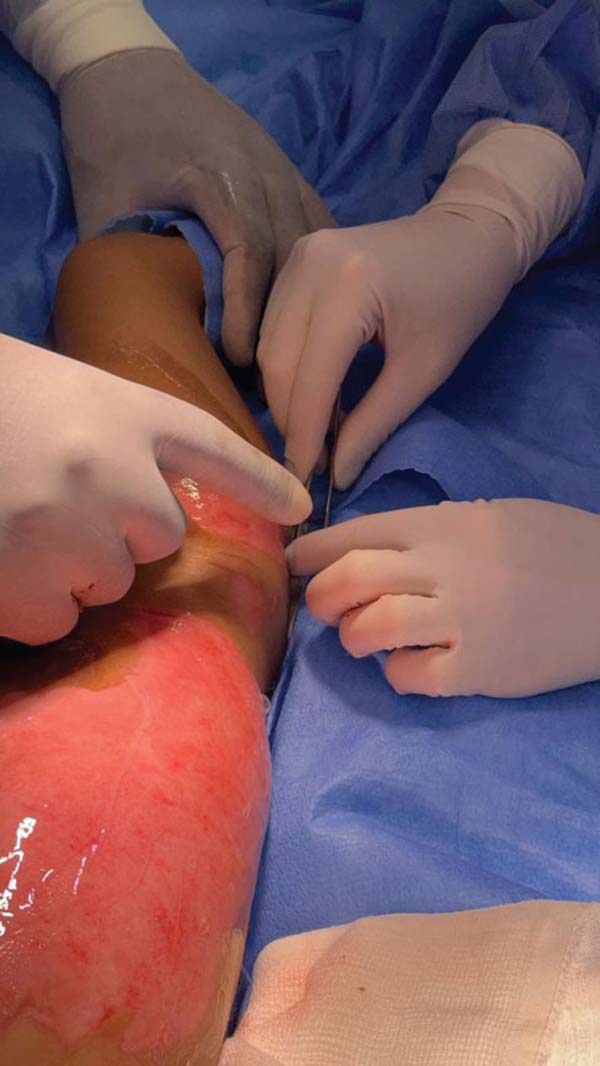
O primeiro transplante de MA legalizada foi realizado em 5 de novembro de 2025 no Hospital Dom Vicente Scherer. A aplicação foi realizada em um caso de lesão cutânea complexa em paciente adulto. Na mesma data, o biomaterial foi aplicado com sucesso em um paciente pediátrico vítima de
queimadura, no Hospital da Criança Santo Antônio. As ►Figs. 3–4 a 5 mostram a utilização da MA nestes dois casos iniciais.
Discussão
O uso da MA como transplante legalizado no Brasil representa um avanço significativo na incorporação de terapias biológicas ao arsenal cirúrgico nacional. A Portaria GM/MS n° 8.244/2025 permite que bancos de tecidos devidamente habilitados realizem a captação, processamento e distribuição da MA com finalidade terapêutica, fora do escopo experimental.3 Isso significa que o tecido pode ser utilizado como enxerto biológico em procedimentos clínicos rotineiros, com respaldo técnico e jurídico, desde que atendidos os critérios de qualidade microbiológica, rastreabilidade e conformidade documental.
Diferentemente de usos anteriores restritos a protocolos de pesquisa ou importações pontuais, o transplante legalizado insere a MA na prática assistencial regular, ampliando o acesso a um biomaterial com propriedades anti-inflamatórias, epitelizantes e imunomoduladoras, especialmente útil em queimaduras, feridas complexas e reconstruções cutâneas.4 Essa mudança normativa não apenas fortalece a segurança do paciente e a padronização dos procedimentos, mas também abre espaço para estudos multicêntricos e análises de custo-efetividade em larga escala.
O alcance de 13 captações e a liberação de mais de 4.157 cm2 em apenas 50 dias demonstram a robustez do protocolo de captação e processamento, bem como a alta demanda clínica reprimida para a utilização da MA. A alta taxa de utilização (60% do estoque distribuído) corrobora a necessidade atual de curativos biológicos com suas propriedades. Estudos demonstram que a aplicação precoce em queimaduras de espessura parcial pode reduzir a profundidade da lesão, modular a resposta cicatricial e diminuir a necessidade de desbridamento cirúrgico e enxertia autóloga, gerando um benefício econômico e de morbidade para o paciente.5 Além disso, a MA proporciona uma cobertura que alivia a dor e confere um ambiente ideal para a regeneração.6 O sucesso de 100% no controle de qualidade (ausência de contaminação) encontrado neste estudo atesta a eficácia dos protocolos, desde a triagem da doadora até o processamento final. A segurança microbiológica é um pilar da terapia de transplantes e é um pré-requisito para o uso clínico generalizado da MA.
A aplicação pioneira em pacientes adultos e pediátricos ressalta a versatilidade clínica do tecido. O caso pediátrico, em particular, sublinha a importância da MA no manejo de queimaduras em crianças, onde minimizar a dor e acelerar a cicatrização é essencial para evitar a contratura e otimizar o resultado funcional e estético a longo prazo.
Estudos prévios têm consistentemente demonstrado que a aplicação da MA favorece a aceleração do processo de cicatrização e reduz a necessidade de procedimentos mais invasivos.7 A MA é um curativo biológico que tem se mostrado custo-efetivo no tratamento de queimaduras promovendo angiogênese, organização do colágeno e regeneração epitelial.8
A análise comparativa entre os dados iniciais da MA e os indicadores consolidados da pele alógena no BTDRCC sugere um diferencial operacional potencialmente relevante. Enquanto o tempo médio de processamento e liberação da pele gira em torno de 45 dias, o intervalo observado para a MA foi de aproximadamente 12,5 dias. Além disso, a taxa de descarte por contaminação microbiológica na pele é historicamente próxima de 25%, ao passo que, nas captações iniciais da MA, observou-se uma taxa de descarte de 0%. Embora esses dados ainda não permitam conclusões definitivas, eles apontam para uma possível maior eficiência microbiológica e operacional, o que pode representar um caminho promissor para ampliar a oferta de tecidos biológicos em contextos de escassez. Estudos prospectivos e multicêntricos serão fundamentais para validar essas observações e estabelecer parâmetros comparativos mais robustos.
As limitações dessa nota prévia incluem não apresentar dados de seguimento clínico (tempo de cicatrização, taxa de enxertia, qualidade da cicatriz, índice de complicações). No entanto, o objetivo de validar a implementação logística e a capacidade produtiva foi alcançado. Os próximos passos da nossa equipe incluem o monitoramento prospectivo dos desfechos clínicos e uma análise econômica rigorosa. A avaliação de custo-benefício é fundamental para justificar a expansão e sustentabilidade do programa no Sistema Nacional de Transplantes. Espera-se que a redução da morbidade, do tempo de internação, da necessidade de reintervenções e redução de custos consolidem a MA como uma opção terapêutica eficiente no cenário brasileiro.
Conclusão
Nos 50 dias iniciais de implementação, o protocolo estabelecido resultou na liberação de 4.157 cm2 de membrana amniótica apta para enxertia, com 100% de conformidade microbiológica. Esses resultados preliminares evidenciam não apenas a viabilidade operacional e a segurança do processo, como também destacam o caráter inovador do aproveitamento de um tecido de anexo fetal que geralmente é descartado após o parto.
A experiência do BTDRCC demonstra que a MA pode configurar-se como recurso estratégico no cuidado a pacientes com feridas complexas, em especial queimaduras, abrindo espaço para uma atuação integrada entre cirurgia plástica, obstetrícia, equipes de queimados e demais especialidades envolvidas nesses cuidados de alta morbidade. Essa articulação interprofissional fortalece a linha de cuidado desde a gestação e o parto, com captação planejada e segura do tecido, até sua aplicação clínica em cenários de alta complexidade.
A divulgação ampla desse programa, tanto entre profissionais de saúde quanto para a população em geral, é fundamental para ampliar o conhecimento sobre a segurança e os benefícios da MA e, consequentemente, estimular o aumento do número de doadoras. Ao transformar um tecido habitualmente não aproveitado em um enxerto biológico de elevado valor terapêutico, o sistema de saúde incorpora uma alternativa efetiva e socialmente relevante, com um potencial impacto na redução de morbidade, tempo de internação e necessidade de procedimentos cirúrgicos adicionais. Estes dados preliminares validam a viabilidade operacional e a segurança da terapia e estabelecem a base para futuras investigações sobre desfechos clínicos e a análise de custos do uso da MA por cirurgiões plásticos no Brasil.
REFERENCES
1. https://doi.org/10.3390/pharmaceutics15030748
2. https://doi.org/10.1097/TA.0000000000003050
3. Brasil. Ministério da Saúde. Portaria n° 8.244, de 25 de setembro de 2025. Atualiza as Tabelas de Serviço Especializado e habilitações do Cadastro Nacional de Estabelecimentos de Saúde (CNES) e inclui e altera Procedimentos, relacionados a Transplante Pediátrico e Banco de Multitecidos na Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do SUS (Tabela de Procedimentos do SUS) Brasília: Diário Oficial da União; 2025. Available from: https://www.in.gov.br/web/dou/-/portaria-gm/ms-n-8.244-25-de-setembro-de-2025-658712781
4. https://doi.org/10.1016/j.bjps.2022.08.028
5. https://doi.org/10.1007/s12015-025-10892-x
6. https://doi.org/10.3390/jcm14124272
7. https://doi.org/10.1111/srt.13860
8. https://doi.org/10.1016/j.burns.2025.107522
1. Banco de Tecidos Humanos Dr. Roberto Corrêa Chem, Hospital Santa Casa de Porto
Alegre, Porto Alegre, RS, Brasil
2. Hospital Santa Casa de Porto Alegre, Centro Histórico, Porto Alegre, RS, Brasil
3. Maternidade, Hospital Santa Casa de Porto Alegre, Centro Histórico, Porto Alegre,
RS, Brasil
Disponibilidade dos Dados
Suporte Financeiro
Endereço para correspondência Eduardo Mainieri Chem, Hospital Santa Casa de Porto Alegre, Banco de Tecidos Humanos Dr. Roberto Corrêa Chem, Rua Professor Annes Dias, 295, Centro Histórico, Porto Alegre – RS, Brasil. CEP: 90020-090 (e-mail: eduardo@chem.com.br).
Article received: December 10, 2025.
Article accepted: December 16, 2025.
Conflito de Interesses Os autores não têm conflito de interesses a declarar.
Editor-chefe: Dov Charles Goldenberg.





 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter