
Review Article - Year 2016 - Volume 31 -
Tratamento geral e das feridas na epidermólise bolhosa hereditária: indicação e experiência usando curativo de hidrofibra com prata
General treatment and wound management in hereditary epidermolysis bullosa: indication and experience using silver hydrofiber dressing
RESUMO
INTRODUÇÃO: Epidermólise bolhosa (EB) hereditária é uma desordem rara caracterizada pela fragilidade cutaneomucosa, com formação de bolhas ao mínimo trauma. O tratamento consiste em suporte clínico, nutricional, manejo da dor e das lesões cutâneas. A hidrofibra com prata (Aquacel Ag®) é um tipo de curativo de fibra de carboximetilcelulose e prata que pode ser utilizada em casos selecionados de EB.
OBJETIVO: Revisão da literatura sobre o tratamento geral e o manejo das lesões cutâneas na EB congênita, além de avaliar a indicação e experiência usando curativo de hidrofibra com prata.
MÉTODOS: A revisão incluiu artigos originais e revisões sistemáticas, publicados entre 2009 e 2014. Selecionamos ainda dois pacientes com EB congênita tratados na Divisão de Cirurgia Plástica do Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo.
RESULTADOS: Há escassez de evidências científicas relacionadas ao tratamento das lesões cutâneas na EB congênita, sendo a maioria das recomendações baseadas em opiniões de especialistas. A hidrofibra está indicada na maioria dos consensos para feridas com alguma exsudação e mostrou-se mais absorvente que o alginato. Em nossa experiência, houve aparente melhor controle da dor, do sangramento e da hipotermia com o uso da hidrofibra, que apresenta a vantagem de não necessitar de trocas diárias, podendo permanecer na ferida por até duas semanas.
CONCLUSÕES: O tratamento geral e das lesões na EB é um desafio. A hidrofibra com prata é uma opção de tratamento para as feridas na EB hereditária, sem necessidade de trocas diárias de curativo.
Palavras-chave: Epidermólise bolhosa; Terapêutica; Ferimentos e lesões; Curativos oclusivos; Compostos de prata.
ABSTRACT
INTRODUCTION: Hereditary epidermolysis bullosa (EB) is a rare disorder characterized by cutaneomucous fragility, with formation of blisters during minimal trauma. Treatment consists of clinical and nutritional support and management of pain and skin lesions. Silver hydrofiber (Aquacel Ag®) is a type of carboxymethylcellulose fiber dressing with silver that can be used in selected cases of EB.
OBJECTIVE: To review the literature on the general treatment and management of cutaneous lesions in congenital EB and evaluate the indication and experience of using silver hydrofiber dressing.
METHODS: The review included original articles and systematic reviews published between 2009 and 2014. We also selected two patients with congenital EB treated at the Plastic Surgery Division of Hospital das Clínicas of the Faculty of Medicine of Ribeirão Preto at the University of São Paulo.
RESULTS: There is a shortage of scientific evidence related to the treatment of skin lesions in congenital EB, with most recommendations being based on expert opinions. Hydrofiber is indicated in most consensuses for wounds with some exudation and has been shown to be more absorbent than alginate. In our experience, there was apparent improved control of pain, bleeding, and hypothermia with the use of hydrofiber, which has the advantage of not requiring daily changes and can remain on the wound for up to two weeks.
CONCLUSIONS: The general and lesion treatments in EB are challenging. Hydrofiber with silver is a treatment option for wounds in hereditary EB, without the need for daily dressing changes.
Keywords: Epidermolysis bullosa; Therapeutics; Wounds and lesions; Occlusive Dressings; Silver compounds.
A epidermólise bolhosa (EB) faz parte de um grupo de doenças hereditárias caracterizado pela fragilidade cutânea com formação de bolhas ao mínimo trauma, causada por mutações em diversas proteínas estruturais da pele. É classificada em quatro tipos, dependendo da localização da proteína mutada: simples, juncional, distrófica e síndrome de Klinder. Há vários subtipos de acordo com a mutação ocorrida. O diagnóstico laboratorial da EB é realizado por biópsia de pele e mapeamento por imunofluorescência, microscopia eletrônica e análise das mutações1.
Há descritas mais de 1000 diferentes mutações envolvendo 14 genes estruturais. As mutações causam menor produção de proteínas responsáveis pela adesão dermoepidérmica, levando à formação de bolhas em um plano de clivagem uniforme. A gravidade da doença dependerá da proteína mutada e do grau da mutação2. A EB é doença rara, com estimativa de prevalência de 8,22 por 1 milhão de pessoas e a incidência de 19,6 por 1 milhão de nascidos vivos. Não há predileção racial ou geográfica3.
O manejo das lesões da EB é um desafio dentro da Medicina devido à complexidade e variedade das suas manifestações. A Cirurgia Plástica apresenta importante papel no tratamento das feridas complexas na EB.
OBJETIVO
O objetivo deste trabalho é revisar o tratamento geral e das lesões cutâneas na EB congênita, além de avaliar as indicações e eficiência da hidrofibra com prata e relatar a experiência de dois pacientes consecutivos com EB tratados em nosso serviço.
MÉTODOS
Foi realizada revisão da literatura na base de dados PubMed/Medline, incluindo artigos originais e revisões publicados entre 2009 e 2014. Os descritores utilizados foram: "epidermolysis bullosa", isolado ou associado com "congenital"; "therapy"; "wound care"; "inherited"; "hydrofiber". Foram selecionados os artigos mais relevantes e as recomendações foram agrupadas de forma a resumir as recomendações desses estudos, principalmente relacionadas ao manejo geral e das lesões.
Além disso, relatamos o caso de dois pacientes consecutivos com EB tratados na Divisão de Cirurgia Plástica do Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo (HCFMRP-USP), a conduta adotada e o tratamento com a utilização de hidrofibra com prata (Aquacel Ag® - Convatec®).
RESULTADOS
Recomendações gerais
Diante da suspeita de um recém-nascido com EB, deve-se imediatamente identificar o tipo de lesão realizando um mapeamento das áreas acometidas e documentação fotográfica. O cálculo da superfície acometida pode ser estimado com os mesmos métodos utilizados para pacientes queimados4. O seguimento regular do paciente deve ser realizado com avaliação de todo corpo à procura de novas lesões, incluindo couro cabeludo, orelha externa, cavidade oral, região genital e anal5.
Alguns cuidados gerais com os recém-nascidos devem ser tomados: proteger as proeminências ósseas; evitar incubadora, já que o calor pode levar à formação de bolhas; evitar grampos umbilicais, preferindo por ligadura com fio; evitar aspiração excessiva de naso e orofaringe, porém, se for extremamente necessária, utilizar cateteres macios e com baixa pressão; retirar os adesivos dos eletrodos e fixá-los com curativo não aderente; usar coxim abaixo dos aparelhos de pressão.
As roupas devem ser de fácil vestimenta e não devem conter costura. Algumas opções no mercado como Dermasilk® possuem ação antimicrobiana e podem ser utilizadas. Fraldas não devem conter elásticos e aquelas com velcro evitam que as partes adesivas colem na pele. Evitar manipulação excessiva do recém-nascido e, quando o transporte for necessário, o bebê deve ser segurado com uma mão do cuidador atrás do pescoço e outra nas nádegas, evitando fricção excessiva. Em bebês que amamentam, aplicar parafina na aréola e mama para evitar trauma pelo reflexo de procura5.
a) Cuidados com a área da fralda: Pode ser higienizada com parafina líquida ou emoliente a base óleo a cada troca. Também pode ser utilizado curativo primário com silicone macio como Mepitel® ou hidrogel; para lesões muito exsudativas, pode ser usado antissépticos ou espumas de silicone como Mepilex®5.
b) Banho: Não utilizar substâncias tóxicas. Pode ser realizado com solução salina ou água. Ácido acético em concentração de 0,25 a 1% pode ser utilizado com objetivo de melhor controle bacteriano6. O banho deve ser em água morna. Em lesões muito infectadas, pode ser acrescentada clorexidina 0,1%. Em lesões crostosas, podem ser usados emolientes ou óleos. A frequência do banho deve ser individualizada de acordo com o tipo e curativo utilizado7,8.
c) Manejo das bolhas: Novas bolhas devem ser puncionadas e drenadas para evitar dissecção e extensão da mesma, entretanto, a pele da bolha pode ser mantida para facilitar a reepitelização, evitar infecção e reduzir a dor9,10.
d) Manipulação das crostas: Pele ressecada e com crostas pode ser tratada com emolientes, o que ajuda a reduzir a dor e prurido10. Agentes queratolíticos como ureia e ácido salicílico podem ser usados para tratamento da hiperceratose palmo-plantar, porém cuidados especiais devem ser tomados em crianças pequenas11.
e) Cuidados com as mucosas: Conjuntiva deve ser regularmente lubrificada com lanolina e colírios sem conservantes ou gel contendo ácido hialurônico, polietileno ou propilenoglicol. Além disso, lubrificação nasal deve ser realizada constantemente com produtos contendo vitamina E ou simplesmente vaselina12.
f) Estado nutricional: O paciente com EB em seus subtipos mais graves é cronicamente desnutrido por vários motivos: disfagia devido ulceração de mucosa oral e esofágica, microstomia, anquiloglossia, perdas dentárias e consumo catabólico pelas lesões abertas. Assim, o suporte nutricional deve ser precoce, principalmente nos casos graves de EB. A dieta deve ser hipercalórica (100-150% das necessidades) e hiperproteica (115-200% das necessidades)13.
A suplementação de ferro oral ou intravenosa está indicada em casos de anemia microcítica. Uso combinado de ferro com eritropoietina foi proposto em um artigo14. Algumas outras vitaminas podem ser repostas após avaliação e individualização para casa caso como, por exemplo, vitaminas A, C, D, E, zinco, cálcio, carnitina, selenium15.
A nutrição enteral por sonda não deve ser usada por tempo prolongado, pois pode provocar erosões no esôfago e orofaringe. Quando necessária, deve ser macia e de tamanho pequeno. Maximização da nutrição é de vital importância para promover crescimento e desenvolvimento da criança, além de otimizar a cicatrização das lesões16. Em alguns casos, gastrostomia deverá ser indicada para manter um aporte nutricional adequado, porém em casos graves, como na EB juncional tipo Herlitz, não está indicada em contexto paliativo6.
g) Tratamento da anemia: No portador de EB, a anemia é de causa multifatorial. Há trabalhos que recomendam manter uma hemoglobina maior que 8 mg/dl6. É descrito que níveis de hemoglobina menor que 10 mg/dl podem prolongar o tempo de cicatrização de úlceras venosas devido à redução da oxigenação17. Níveis baixos de hemoglobina em pacientes com EB estão relacionados com atraso na cicatrização das lesões. Suplementação oral de ferro pode ser realizada associada ou não à eritropoietina18,19. Transfusões sanguíneas podem ser indicadas se os níveis de hemoglobina de encontram abaixo de 8 mg/dl ou para pacientes que não respondem a outras medidas6.
h) Alívio do prurido: Prurido é um sintoma que compromete muito a qualidade de vida do paciente e é comum na EB e de difícil mensuração em crianças pequenas devido a incapacidade de comunicação. Em crianças maiores e em adultos, pode ser tratado com antihistamínicos como hidroxizine, loratadina, cetirizine. Em prurido persistente, há relato de tratamento com ondasetron e baixas doses de gabapentina20.
i) Manejo da dor: Dor é o sintoma mais comum na EB. O controle da dor deve fazer parte do cuidado diário com o bebê já que, no caso de EB hereditária, a dor está presente desde o nascimento. A atuação deve ser individualizada para cada paciente e é necessário considerar o tipo de dor.
A mensuração da intensidade da dor é realizada por escalas próprias para idade. A dor pode ser aguda, crônica ou neuropática. O componente psicológico pode estar presente em crianças maiores. A abordagem da dor deve ser tanto preventiva, evitando traumas, disseminação das bolhas e infecção local, quanto terapêutica. Na condução terapêutica, o tratamento pode ser farmacológico ou não farmacológico6.
Devemos lembrar que os momentos de dor mais intensa estão vinculados à manipulação do paciente como no banho e nas trocas de curativos. Portanto, medicações devem ser feitas antes desses procedimentos e o tipo de medicação irá depender do tipo de dor e idade do paciente.
Anestésicos tópicos podem ser usados para minimizar a dor durante curativos e punções venosas, porém deve-se atentar para doses tóxicas. Analgésicos comuns como paracetamol são os escolhidos em caso de dor leve à moderada. Para quadro álgico mais intenso, durante procedimentos de manipulação, poderão ser utilizados os opioides associados ou não a hidroxizine e midazolan para controle da ansiedade e breve sedação.
Em crianças, a ketamina, mais raramente, é utilizada nas trocas de curativos21. No caso de dor crônica, anti-inflamatórios não hormonais podem ser utilizados. Em casos de dor neuropática, pode-se associar pregabalina, gabapentina ou antidepressivos tricíclicos. No caso de dor aguda, além de paracetamol e opioides, são descritos bloqueios anestésicos locais e aplicação de toxina botulínica para relaxamento do esfíncter anal em caso de erosões e fissuras. Para crianças menores de 2 anos, é descrito o uso de sucrose 24% oral, que promove uma analgesia de curta duração5,6,22,23.
Categorias de curativos
A escolha do curativo varia de acordo com o local das lesões e disponibilidade dos produtos6,9,10,23,24. Existem produtos que diminuem a frequência de trocas de curativos, reduzindo a dor e manipulação, o que também diminui o risco de formação de bolhas e infecção. Curativos não adesivos reduzem a dor no momento da remoção.
Em contrapartida, algumas revisões sistemáticas da literatura mostraram apenas pequena vantagem dos curativos avançados (hidrogéis, hidrofibras e espumas) quando comparados com gazes embebidas em parafina para úlceras crônicas não relacionadas com EB25.
Antibióticos e antissépticos são úteis e têm seu papel comprovado no tratamento de infecção superficial em úlceras crônicas. Alguns curativos como hidrogel, hidrofibra e membranas poliméricas são úteis no desbridamento de tecido desvitalizado. Porém, em caso de lesões múltiplas ou lesões profundas, pode ser necessário desbridamento cirúrgico com anestesia5.
Há no mercado um grande número de curativos para tratamento das lesões da EB e para cada caso devem-se individualizar as indicações, uma vez que não há um curativo ideal.
a) Espuma: é geralmente composta de poliuretano hidrofílico e algumas contêm silicone para reduzir a aderência. Possui uma membrana semipermeável que possibilita a drenagem do exsudato. Dependendo da quantidade de exsudato, pode permanecer até 7 dias, porém requer troca contínua do curativo secundário. Exemplos: Mepilex®, Mepilex Lite®, Mepilex Border®, Mepilex Border Lite® e Polymem®5,6,24,26.
b) Hidrogel: feito de polímeros insolúveis que expandem na presença de água, hidratando a ferida e promovendo desbridamento autolítico. Está indicado para feridas com pouca ou nenhuma exsudação. Melhora dor, prurido e desconforto. Exemplos: Duoderm®, Intrasite®, Sheets®, ActFoamCool® e Intrasite Conformable®5,6,24,26,27.
c) Alginato: é produzido por fibras de algas e transforma-se em um gel não adesivo quando em contato com exsudado. Indicado em feridas com exsudação, associado ou não com íons de cálcio (que promovem hemostasia)5,6,28.
d) Curativos absorventes modificados: finas camadas de fibra de algodão absorvente que são colocadas sobre placas de tereftalato de polietileno e com os bordos vedados com plástico, impedindo aderência das vestimentas na ferida e a superfície perfurada permite a passagem de exsudado pelo curativo. É relativamente barato e não aderente. Exemplos: Telfa®, Restore®, ETE® e Mesorb®5,6,24,26.
e) Camada de contato: feito de material inerte e possui remoção atraumática. Exemplos: Mepitel®, Silflex®, Mepitac®, Adaptic touch®5-7.
f) Celulose biossintética: curativo constituído de celulose, água e 0,085% de gluconato de clorexidina. Tem função tanto de absorver como de hidratar. Reduz dor e prurido. Exemplo: Suprasorb X®5,6.
g) Curativos de lipidocoloide: composto de malha de poliéster impregnada por polímeros de hidrocoloide e vaselina. Quando em contato com o exsudado, os polímeros de hidrocoloide são hidratados e constituem, com a vaselina, uma interface de lipidocoloide, promovendo um curativo não aderente. Está indicado em feridas com exsudado e também para proteção de áreas vulneráveis5,6.
h) Hidrofibras: São compostas por carboximetilcelulose que, quando em contato com exsudado, transforma-se em gel. São mais absorventes que os alginatos. Indicadas em feridas exsudativas e criticamente colonizadas ou infectadas. O Aquacel Ag® é uma associação de hidrofibra com a prata, que tem função de controle da infecção. Produtos contendo prata devem ser utilizados com cautela, principalmente em crianças, devido a potencial toxicidade pela absorção, e níveis séricos devem ser dosados em caso de uso prolongado. Possui limitação do uso em feridas com pouca ou nenhuma exsudação ou com crostas5,6,9,27.
Escolha do curativo de acordo com as características das lesões
a) Feridas secas ou levemente exsudativas: curativos de silicone não adesivo ou placas de lipidocoloide; fina e macia camada de poliuretano siliconado e hidrogéis. Hidrogéis podem ser trocados diariamente, enquanto os outros tipos podem ser trocados a cada 3-4 dias5-7,9,27.
b) Feridas muito exsudativas: nestes casos, curativos com hidrofibra ou com espuma de silicone superabsorvível são preferidos. Além disso, esponjas macias de silicone e membranas poliméricas são indicadas. Alguns desses curativos precisam de um outro curativo secundário, uma vez que não aderem bem5-9.
c) Feridas criticamente colonizadas e infectadas: o diagnóstico de infecção das lesões pode ser dado por alguns parâmetros: demora na cicatrização, aumento do tamanho ou da quantidade de exsudado, presença de debris e/ou tecido necrótico, odor forte, avaliação se há edema, eritema e aumento da temperatura. Na presença dos critérios acima, alguns trabalhos sugerem colher swab e realizar tratamento de acordo com culturas, enquanto outros indicam uso de hidrofibra, alginato e antibióticos para esse tipo de ferida5-7,9,24.
d) Prurido e dor: celulose biossintética e hidrogel podem ser usados em feridas que necessitam do controle da dor e prurido. Além disso, corticoides tópicos de media potência podem ser utilizados5,6,9.
e) Hipergranulação: curativos com antibióticos e anti-inflamatórios podem ser benéficos. Também corticosteroides tópicos podem ser utilizados em curto período5-7.
RELATO DOS CASOS
No ano de 2014 foram admitidos, simultaneamente, dois pacientes com EB na Unidade de Terapia Intensiva pediátrica da Unidade de Emergência do HCFMRP-USP. A Divisão de Cirurgia Plástica foi solicitada para colaborar no tratamento desses pacientes com feridas complexas decorrentes da EB.
Um paciente do sexo masculino de 2 meses (Figuras 1, 2 e 3) e um do sexo feminino de 6 meses de idade apresentavam diagnóstico de EB do tipo juncional, acometendo cerca de 38% da superfície corporal no primeiro e 35% no segundo paciente. As lesões acometiam cabeça, incluindo boca, membros, tronco, períneo, mucosas e leitos ungueais. Caracterizavam, portanto, casos graves da doença com prognóstico muito reservado e sobrevida baixa. As lesões mostravam-se muito exsudativas.
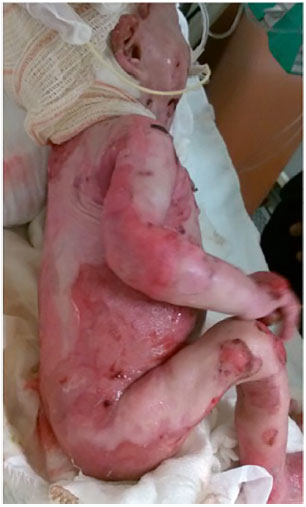
Figura 1. Feridas em tronco e membros de paciente com epidermólise bolhosa - visão lateral direita.
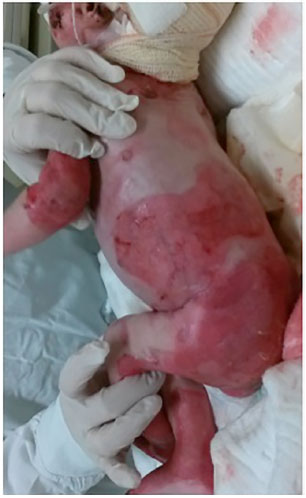
Figura 2. Feridas em tronco e membros de paciente com epidermólise bolhosa - visão lateral esquerda.
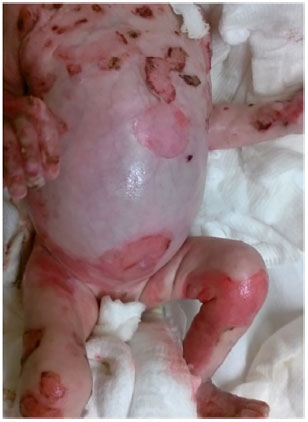
Figura 3. Feridas em tronco e membros de paciente com epidermólise bolhosa - visão anterior.
Dentre as opções disponíveis em nossa instituição, optamos pelo uso da hidrofibra com prata (Aquacel Ag®), uma vez que este curativo está indicado em lesões exsudativas e a prata teria benefício no controle da infecção, além de não necessitar de trocas diárias (Figuras 4 e 5). Nestes casos, as trocas de curativos foram feitas de acordo com a saturação dos mesmos.
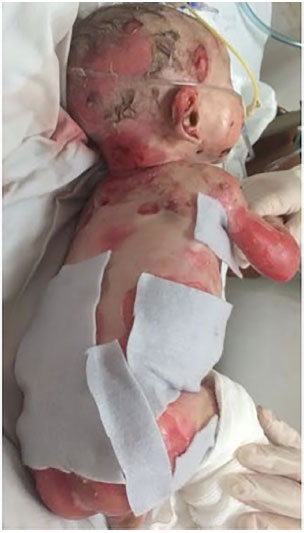
Figura 4. Curativo das feridas usando hidrofibra com prata - visão lateral direita.
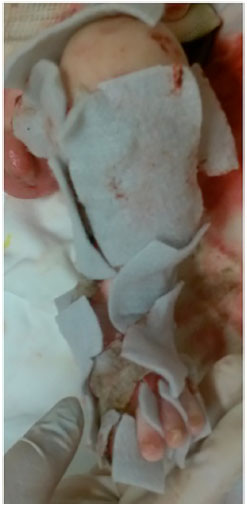
Figura 5. Curativo das feridas usando hidrofibra com prata - detalhe do membro inferior esquerdo.
Após início do curativo com a hidrofibra com prata, notamos que houve melhora da hipotermia, já que em algumas áreas os curativos não demandavam troca diária. Também houve redução do sangramento e aparente melhor controle da dor durante as trocas. Pudemos observar a cicatrização de algumas regiões como tronco e membros após utilização da hidrofibra.
Porém, o curativo mostrou-se limitado para tratamento da região perineal, pela constante contaminação e saturação das lâminas de hidrofibra, com necessidade de trocas mais constantes. Os dois pacientes foram a óbito por sepse entre a terceira e a quarta semana após o início dos curativos.
Perspectivas
Alguns artigos têm relatado o uso de terapia genética, introduzindo genes em cultura de queratinócitos de pacientes portadores de EB seguido de autoenxerto. Também se tem estudado a transferência através de vetores retrovirais contendo genes para expressão de colagénio tipo VII em ratos imunodeficientes. Transplante de medula óssea e sangue alogênico também estão sendo testados para tratamento da EB distrófica com alguns resultados promissores, porém necessitando de estudos mais consistentes para serem utilizados em maior escala29-31.
DISCUSSÃO
A EB é uma doença complexa, muitas vezes letal, e com devastador efeito na qualidade de vida dos portadores que sobrevivem. As manifestações clínicas variam de acordo com cada subtipo da doença. O tratamento global da doença envolve terapia nutricional, manejo da dor e da anemia, prevenção de lesões, tratamento das lesões vigentes além do apoio psicológico do paciente e dos familiares.
O tratamento das lesões cutâneas é um desafio para as equipes de saúde devido ao seu caráter crônico e recidivante. Há escassez de evidências científicas, sendo a maioria das recomendações baseadas em opiniões de especialistas e relatos de caso. Há muitas opções no mercado de produtos destinados ao tratamento das lesões decorrentes da EB. Não existe um curativo ideal e a escolha deve ser individualizada e baseada nas características de cada lesão, idade do paciente e recursos disponíveis.
Para feridas secas ou levemente exsudativas, a maioria dos estudos orientam hidrogel, lipidocoloide ou placas de silicone não aderentes. Já em lesões exsudativas podem ser utilizados alginato, hidrofibra e espumas de silicone. Em lesões infectadas, pomadas antibióticas como sulfadiazina de prata podem ser usadas ou antibioticoterapia parenteral guiada por cultura.
A hidrofibra com prata é indicada para lesões exsudativas ou infectadas e, em nossa experiência, foi útil para controle da hipotermia e, possivelmente, da dor, já que diminuiu a frequência da troca de curativos. Uma limitação encontrada para seu uso foi na região perineal, devido à presença frequente de urina e fezes, com rápida saturação das placas e necessidade de trocas mais frequentes.
CONCLUSÃO
O tratamento geral e das lesões na EB é um desafio. O manejo dos pacientes deve ser individualizado de acordo com a apresentação da doença e ter como objetivo minimizar sequelas físicas e psicológicas. A hidrofibra com prata é uma opção de tratamento para essas feridas, útil para o controle da hipotermia e sem necessidade de trocas diárias de curativo.
COLABORAÇÕES
FBC Análise e/ou interpretação dos dados; concepção e desenho do estudo; realização das operações e/ou experimentos; redação do manuscrito ou revisão crítica de seu conteúdo.
PSC Análise e/ou interpretação dos dados; aprovação final do manuscrito; redação do manuscrito ou revisão crítica de seu conteúdo.
JAFJ Análise e/ou interpretação dos dados; aprovação final do manuscrito; concepção e desenho do estudo; redação do manuscrito ou revisão crítica de seu conteúdo.
REFERÊNCIAS
1. Intong LR, Murrell DF. Inherited epidermolysis bullosa: new diagnostic criteria and classification. Clin Dermatol. 2012;30(1):70-7.
2. Fine JD. Inherited epidermolysis bullosa: recent basic and clinical advances. Curr Opin Pediatr. 2010;22(4):453-8.
3. Fine JD, Johnson LB, Suchindran C, Moshell A, Gedde-Dahl T. The epidemiology of inherited EB: findings within American, Canadian, and European study populations. In: Fine JD, Bauer EA, McGuire J, Moshell A, eds. Epidermolysis Bullosa: Clinical, Epidemiologic, and Laboratory Advances, and the Findings of the National Epidermolysis Bullosa Registry. Baltimore: Johns Hopkins University Press; 1999. p. 101-13.
4. Hettiaratchy S, Papini R. Initial management of a major burn: II-assessment and resuscitation. BMJ. 2004;329(7457):101-3.
5. El Hachem M, Zambruno G, Bourdon-Lanoy E, Ciasulli A, Buisson C, Hadj-Rabia S, et al. Multicentre consensus recommendations for skin care in inherited epidermolysis bullosa. Orphanet J Rare Dis. 2014;9:76.
6. Pope E, Lara-Corrales I, Mellerio J, Martinez A, Schultz G, Burrell R, et al. A consensus approach to wound care in epidermolysis bullosa. J Am Acad Dermatol. 2012;67(5):904-17.
7. Mellerio JE, Weiner M, Denyer JE, Pillay EI, Lucky AW, Bruckner A, et al. Medical management of epidermolysis bullosa: Proceedings of the IInd International Symposium on Epidermolysis Bullosa, Santiago, Chile, 2005. Int J Dermatol. 2007;46(8):795-800.
8. Mellerio JE. Infection and colonization in epidermolysis bullosa. Dermatol Clin. 2010;28(2):267-9.
9. Denyer J, Pillay E. Best practice guidelines for skin and wound care in epidermolysis bullosa [citado 2016 Nov 22]. Disponível em: http://www.woundsinternational.com/media/issues/623/files/content_10609.pdf
10. Lara-Corrales I, Arbuckle A, Zarinehbaf S, Pope E. Principles of wound care in patients with epidermolysis bullosa. Pediatr Dermatol. 2010;27(3):229-37.
11. Khan MT. Podiatric management in epidermolysis bullosa. Dermatol Clin. 2010;28(2):325-33.
12. Figueira EC, Murrell DF, Coroneo MT. Ophthalmic involvement in inherited epidermolysis bullosa. Dermatol Clin. 2010;28(1):143-52.
13. Haynes L. Nutrition for children with epidermolysis bullosa. Dermatol Clin. 2010;28(2):289-301.
14. Kuo DJ, Bruckner AL, Jeng MR. Darbepoetin alfa and ferric gluconate ameliorate the anemia associated with recessive dystrophic epidermolysis bullosa. Pediatr Dermatol. 2006;23(6):580-5.
15. Fine JD, Johnson LB, Weiner M, Suchindran C. Gastrointestinal complications of inherited epidermolysis bullosa: cumulative experience of the National Epidermolysis Bullosa Registry. J Pediatr Gastroenterol Nutr. 2008;46(2):147-58.
16. Kim KY, Namgung R, Lee SM, Kim SC, Eun HS, Park MS, et al. Nutritional outcomes in children with epidermolysis bullosa: the experiences of two centers in Korea. Yonsei Med J. 2014;55(1):264-9.
17. Keast DH, Fraser C. Treatment of chronic skin ulcers in individuals with anemia of chronic disease using recombinant human erythropoietin (EPO): a review of four cases. Ostomy Wound Manage. 2004;50(10):64-70.
18. Atherton DJ, Cox I, Hann I. Intravenous iron (III) hydroxidesucrose complex for anaemia in epidermolysis bullosa. Br J Dermatol. 1999;140(4):773.
19. Fridge JL, Vichinsky EP. Correction of the anemia of epidermolysis bullosa with intravenous iron and erythropoietin. J Pediatr. 1998;132(5):871-3.
20. Allegaert K, Naulaers G. Gabapentin as part of multimodal analgesia in a newborn with epidermolysis bullosa. Paediatr Anaesth. 2010;20(10):972-3.
21. Saroyan JM, Tresgallo ME, Farkouh C, Morel KD, Schechter WS. The use of oral ketamine for analgesia with dressing change in an infant with epidermolysis bullosa: report of a case. Pediatr Dermatol. 2009;26(6):764-6.
22. Anand KJ; International Evidence-Based Group for Neonatal Pain. Consensus statement for the prevention and management of pain in the newborn. Arch Pediatr Adolesc Med. 2001;155(2):173-80.
23. Pope E, Lara-Corrales I, Mellerio JE, Martinez AE, Sibbald C, Sibbald RG. Epidermolysis bullosa and chronic wounds: a model for wound bed preparation of fragile skin. Adv Skin Wound Care. 2013;26(4):177-88.
24. Denyer JE. Wound management for children with epidermolysis bullosa. Dermatol Clin. 2010;28(2):257-64.
25. Chaby G, Senet P, Vaneau M, Martel P, Guillaume JC, Meaume S, et al. Dressings for acute and chronic wounds: a systematic review. Arch Dermatol. 2007;143(10):1297-304.
26. Gonzalez ME. Evaluation and treatment of the newborn with epidermolysis bullosa. Semin Perinatol. 2013;37(1):32-9.
27. Schober-Flores C. Epidermolysis bullosa: the challenges of wound care. Dermatol Nurs. 2003;15(2):135-8.
28. Powers JG, Morton LM, Phillips TJ. Dressings for chronic wounds. Dermatol Ther. 2013;26(3):197-206.
29. Siprashvili Z, Nguyen NT, Bezchinsky MY, Marinkovich MP, Lane AT, Khavari PA. Long-term type VII collagen restoration to human epidermolysis bullosa skin tissue. Hum Gene Ther. 2010;21(10):1299-310.
30. Wagner JE, Ishida-Yamamoto A, McGrath JA, Hordinsky M, Keene DR, Woodley DT, et al. Bone marrow transplantation for recessive dystrophic epidermolysis bullosa. N Engl J Med. 2010;363(7):629-39.
31. Cutlar L, Greiser U, Wang W. Gene therapy: pursuing restoration of dermal adhesion in recessive dystrophic epidermolysis bullosa. Exp Dermatol. 2014;23(1):1-6.
1. Hospital das Clínicas, Faculdade de Medicina de Ribeirão Preto, Universidade de São Paulo, Ribeirão Preto, SP, Brasil
2. Faculdade de Medicina de Ribeirão Preto, Universidade de São Paulo, Ribeirão Preto, SP, Brasil
Instituição: Faculdade de Medicina de Ribeirão Preto, Universidade de São Paulo, Ribeirão Preto, SP, Brasil.
Autor correspondente:
Jayme Adriano Farina Junior
Av. Bandeirantes, 3900 - Monte Alegre
Ribeirão Preto, SP, Brasil CEP 14048-900
E-mail: jafarinajr@fmrp.usp.br
Artigo submetido: 25/8/2015.
Artigo aceito: 10/2/2016.
Conflitos de interesse: não há.


 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter